Rematurogeneze
Kazuistika
Souhrn: Maturogeneze patří mezi regenerativní endodontické postupy, které se uplatňují zvláště při endodontickém ošetřování stálých zubů s neukončeným vývojem a nekrotickou dření. I přes rozšíření do klinické praxe v posledním desetiletí není známa úspěšnost tohoto ošetření a postup v případě jeho selhání. Tato kazuistika popisuje postup po selhání maturogeneze, a to opakováním léčby s nápravou chyb předchozího ošetření – rematurogenezí.
Klíčová slova: maturogeneze, revaskularizace, revitalizace, zub s neukončeným vývojem
Rematurogenesis
Case report
Summary: Maturogenesis is regenerative end o-dontic procedure which is mostly employed in treating immature permanent teeth with necrotic pulp. Despite the increase in frequency of this treatment modality, the success rate is not known and guideline for solution of treatment failure has not been established yet. This case report deals with treatment of failed maturogenesis which was treated by repeated maturogenesis where the mistakes of previous treatment were rectified.
Key words: maturogenesis, revascularization, revitalization, immature tooth
Úvod
Endodontické ošetření stálých zubů s nedokončeným vývojem patří k nejnáročnějším výkonům v klinické endodoncii. Apexifikace hydroxidem vápenatým vyžaduje velmi dobrou spolupráci pacienta a rodičů, a zvláště u zubů v raných stadiích vývoje je úspěšnost ošetření zpravidla nízká. To je dáno zejména omezeným množstvím tvrdých zubních tkání a zhoršenými mechanickými vlastnostmi dentinu, který je dlouhodobě vystaven působení hydroxidu vápenatého (1). Ve snaze zkrátit dobu léčby a omezit dlouhodobé působení hydroxidu vápenatého se začaly využívat kalciumsilikátové cementy jako tzv. apikální zátka (angl. apical plug) ve spojení s adhezivně fixovanými sklovláknovými čepy (2). V posledních dvou desetiletích došlo k výraznému pokroku v oblasti tkáňového inženýrství a rozšíření znalostí biologie zubní dřeně vedoucí k vytvoření postupů, jejichž cílem je formace nové vitální tkáně uvnitř kořenového systému (3). I když je nepravděpodobné, že by se jednalo o regeneraci, lze předpokládat, že reparativní apozicí tvrdých tkání na vnitřním povrchu zubu dochází ke zvýšení jeho mechanické odolnosti.
Tyto regenerativní endodontické postupy se rozšířily do klinické praxe pod názvy maturogeneze, revaskularizace nebo revitalizace a doporučené postupy ošetření pravidelně vydává Americká asociace endodontistů (AAE) v návaznosti na nově publikované znalosti (4, 5). Pro relativně malou incidenci takto postižených stálých zubů s nedokončeným vývojem není známo přesné indikační spektrum (vývojové stadium zubu, etiologie nekrózy, rozsah a agresivita infekce), úspěšnost ošetření jako takového v závislostech na těchto faktorech, ani parametry, za jakých je vhodné zvolit techniku apikální zátky s využitím kalciumsilikátových cementů. Dále je nutné zmínit, že pokud dojde ke ztrátě stálého zubu s nedokončeným vývojem, a to zvláště ve frontálním úseku, je následná estetická rehabilitace pacienta časově i finančně velmi náročná a vyžaduje komplexní interdisciplinární přístup. Následný výsledek může být, i přes maximální snahu lékařů, kompromisní. Z tohoto pohledu je zlepšení dlouhodobé prognózy takto postižených zubů velmi žádoucí.
V této kazuistice popisujeme případ pacientky, u které bylo primární ošetření maturogenezí neúspěšné a u níž byla opakovaně provedena maturogeneze (tj. rematurogeneze).
Vlastní pozorování
Na počátku března roku 2015 byla odeslána z lékařské služby první pomoci ve Fakultní nemocnici v Olomouci 7letá pacientka k endodontickému ošetření zubu 11 pro akutní periodontitidu. Zub byl na lékařské pohotovosti trepanován a ponechán volně. Pacientka se i s doprovodem dostavila na naše oddělení hned druhý den.
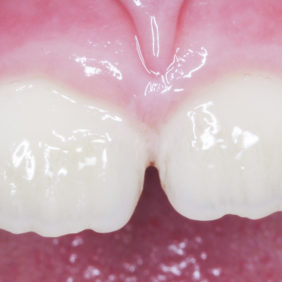
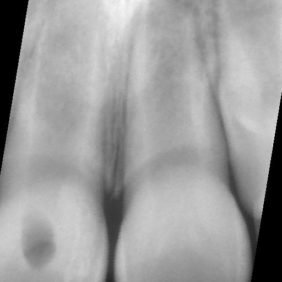
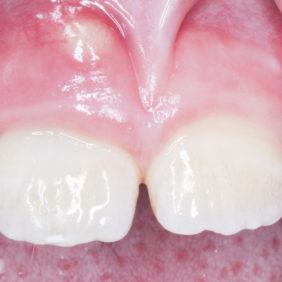
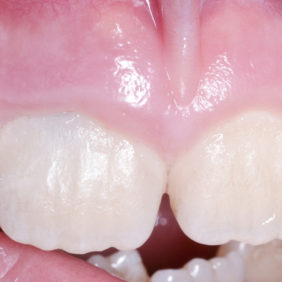
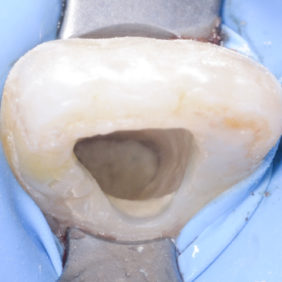
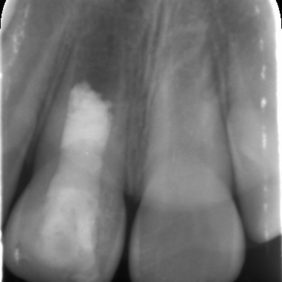
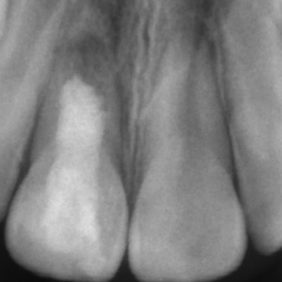
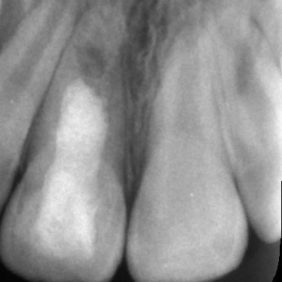
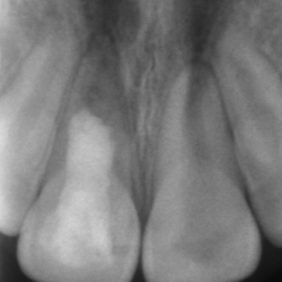
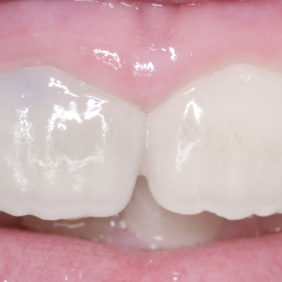
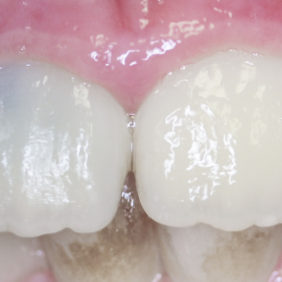
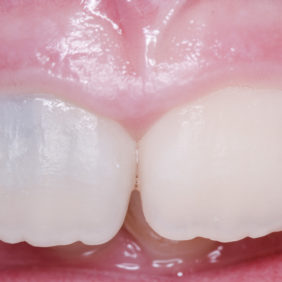
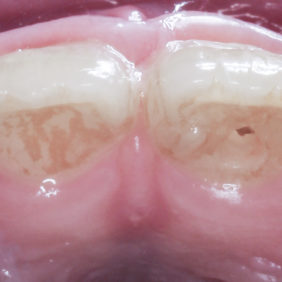
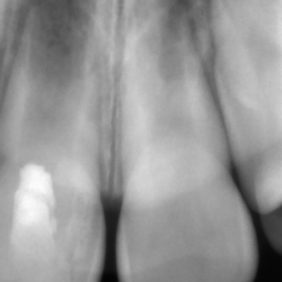
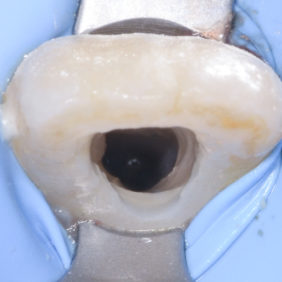
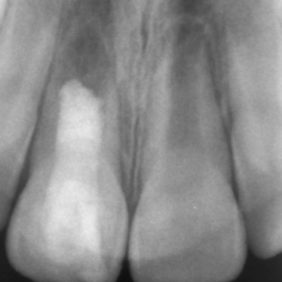
Při klinickém vyšetření jsme nalezli sanovaný smíšený chrup odpovídající věku pacientky (obr. 1), (obr. 2). Zub 11 byl poklepově a palpačně nebolestivý, zkouška vitality chladem nebyla provedena vzhledem k předchozí trepanaci zubu. Dle diagnostického izometrického intraorálního snímku získaného technikou půleného úhlu byl kořen zubu ve druhém vývojovém stadiu dle Cveka, bez známek periapikálního projasnění (obr. 3). Jak z klinického vyšetření, tak z rentgenového snímku bylo zřejmé, že trepanační otvor nebyl dostatečně extendován. Rodiče udávali v rámci anamnézy úraz před zhruba čtyřmi měsíci. Při pádu na ledu došlo k traumatizaci horních středních řezáků a byl přítomen krvavý lem v gingiválním žlábku v okolí klinických korunek zubů. Rodiče pacientky byli motivováni k záchraně zubu a pacientka dobře spolupracovala.
Po vysvětlení jednotlivých možností ošetření zubu 11 (maturogeneze, apexifikace hydroxidem vápenatým nebo zátka z kalciumsilikátového cementu) se rodiče rozhodli pro ošetření maturogenezí. Ošetření maturogenezí bylo provedeno ve dvou návštěvách dle protokolu AAE (5), kdy první fáze ošetření proběhla ihned, ve stejný den.
V infiltrační anestezii 4% articainem (Supracain 4%, Zentiva, Praha, Česká republika) byl na zub nasazen kofferdam, upraven trepanační otvor a pomocí apexlokátoru byla stanovena předběžná pracovní délka. Následně byl zhotoven měřicí snímek s rentgenkontrastním nástrojem. V rámci výplachového protokolu byl využit 1% chlornan sodný po dobu 5 minut a následně byl po vysušení aplikován hydroxid vápenatý (Calxyd, Spofadental, Jičín, Česká republika). Následně byl jako mezivrstva (angl. spacer) využit sterilizovaný teflon a zhotovena provizorní výplň ze skloionomerního cementu.
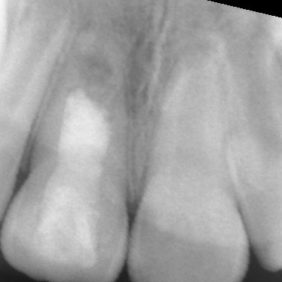
Po dvou týdnech byla provedena druhá fáze ošetření, kdy bylo v rámci výplachu kořenového kanálku využito 20 ml 17% roztoku kyseliny ethylendiaminotetractové (EDTA) po dobu 10 minut. Po výplachu fyziologickým roztokem a vysušení pomocí sterilních papírových čepů bylo indukováno krvácení z periapikální oblasti. Po stabilizaci koagula jsme zhotovili kalciumsilikátovou zátku (ProRoot White MTA, Dentsply-Maillefer, Ballaigues, Švýcarsko) a definitivní adhezivní rekonstrukci. V průběhu druhé fáze ošetření pacientka spolupracovala relativně hůře. Na kontrolním snímku je patrný nedostatečný rozsah trepanačního otvoru, který nezahrnuje meziální roh cavum pulpae (obr. 4). Pacientka byla objednána za jeden měsíc na kontrolní vyšetření k reevaluaci stavu a stanovení dalšího léčebného postupu.
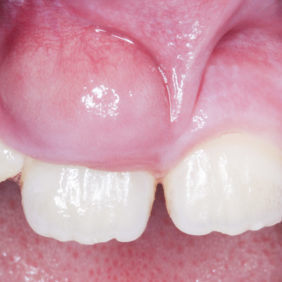
Za dva týdny přichází pacientka s doprovodem pro otok vestibulum oris v místě zubu 11 (obr. 5). Pacientka byla bez zvýšené tělesné teploty (T = 36,2 °C), horní frontální zuby byly poklepově nebolestivé a paradoxně nebyla citlivá ani palpace vestibulárního vyklenutí. V rámci první pomoci bylo provedeno odstranění kompozitní dostavby, rozšíření trepanačního otvoru, výplach 1% chlornanem sodným, aplikace hydroxidu vápenatého do koronální poloviny kořene (Calxyd, Spofadental, Jíčín, Česká republika) a zhotovení provizorní výplně z kapslového skloionomerního cementu.
Při kontrolním vyšetření za dva týdny (obr. 6) a za čtyři týdny (obr. 7) byl postup opakován. V té době bylo možné pozorovat výrazné zmenšování vestibulárního vyklenutí. Při kontrolním vyšetření po čtyřech týdnech byl viditelný cervikální lem dyskolorace, způsobený kalciumsilikátovým cementem (ProRoot White MTA, Dentsply-Maillefer, Ballaigues, Švýcarsko). V této návštěvě byli rodiče opakovaně poučeni o možnostech dalšího ošetření. I přes předchozí neúspěch ošetření maturogenezí se přiklonili k ošetření opakovaným provedením maturogeneze s upraveným léčebným protokolem.
V další návštěvě byl v lokální anestezii 3% mepivacainem (Mepivastezin, 3M ESPE, St. Paul, MN, USA) na zub nasazen kofferdam a odstraněna provizorní skloionomerní výplň. V rámci závěrečného výplachového protokolu bylo využito 10 ml 5% chlornanu sodného po dobu 10 minut, z čehož byl tento výplach 2 minuty aktivován kořenovým nástrojem C-pilot o velikosti ISO 10 (VDW, Mnichov, Spolková republika Německo) upevněným na koncovku Sonicflex (KaVo, Biberach, Spolková republika Německo). Pracovní délka tohoto nástroje byla zkrácena o 3 mm oproti pracovní délce, která byla stanovena s pomocí apexlokátoru a měřicího snímku. Endodontická výplachová kanyla NaviTip (Ultradent, South Jordan, USA) byla taktéž zaváděna na stanovenou pracovní délku zkrácenou o 3 mm. Cílem bylo minimalizovat traumatizaci periapikální oblasti s pravděpodobně přítomnou apikální papilou. Vysoce koncentrovaný, tj. 5% chlornan sodný jsme využili k docílení vyššího proteolytického působení proti extracelulární matrix biofilmu. Abychom zvrátili negativní působení koncentrovaného chlornanu sodného na dentin, prodloužili jsme působení 17% EDTA na dobu 20 minut.
Po výplachu fyziologickým roztokem a vysušení kořenového kanálku sterilními papírovými čepy jsme stimulovali krvácení z periapikákní oblasti. Krevní koagulum jsme stabilizovali s pomocí oxidované celulózy (Traumacel NewDent, Bioster, Veverská Bitýška, Česká republika) (obr. 8). Na takto stabilizované koagulum jsme aplikovali kalciumsilikátovou zátku (ProRoot White MTA, Dentsply-Maillefer, Ballaigues, Švýcarsko) (obr. 9). Následně jsme klinickou korunku adhezivně rekonstruovali a zhotovili kontrolní rentgenový snímek (obr. 10). I přes veškerou snahu o co nejcitlivější kondenzaci kalciumsilikátového cementu došlo k propadnutí kalciumsilikátové zátky zhruba 3 mm pod cementosklovinnou hranici.
V následných kontrolách byl zub 11 klinicky klidný, poklepově a palpačně nebolestivý s negativní reakcí na chlad. Pacientka i doprovod negují bolestivost či otok od provedení rematurogeneze. Kontrolní snímky po třech (obr. 11), šesti (obr. 12), devíti (obr. 13), šestnácti (obr. 14) a dvaceti čtyřech měsících (obr. 15) ukazují pokračující vývoj kořene a apozici mineralizované tkáně na vnitřních stěnách kořene. Periapikální projasnění není přítomno. Cervikální dyskolorace, jež byla přítomna již po prvotním ošetření maturogenezí, se nepatrně zhoršila, avšak klinicky není výrazně rušivá, jak ukazují fotografie z kontrol po šesti (obr. 16), šestnácti (obr. 17) a dvaceti čtyřech měsících (obr. 18).
Diskuze
Nejpravděpodobnější příčinou selhání prvotního ošetření maturogenezí byla reziduální bakteriální infekce, a to buď nedokonale extendovaným trepanačním otvorem, nebo nedokonalou dezinfekcí kořenového kanálku dle protokolu AAE. V literatuře byly popsány i jiné možné příčiny selhání maturogeneze, jako je reinfekce, opakované trauma nebo okluzní trauma (6), jež jsou ale v tomto případě méně pravděpodobné.
V případě selhání maturogeneze neexistuje jasný protokol, podle kterého bychom mohli postupovat. Část autorů doporučuje tyto případy ošetřit konvenčně, plněním kalciumsilikátovým cementem, nebo zub extrahovat. Extrakci zubu ve frontálním úseku se ale snažíme zamezit, jak je to jen možné. Pokud dojde ke ztrátě stálého zubu s nedokončeným vývojem, dochází ke vzniku výrazného kostního defektu, a to zvláště ve frontálním úseku. Následná estetická rehabilitace pacienta je časově i finančně velmi náročná a vyžaduje komplexní interdisciplinární přístup a nezřídka opakované chirurgické výkony včetně augmentace měkkých i tvrdých tkání.
Cílem většiny ošetření dříve selhavších maturogenezí je eliminovat infekci v kořenovém systému zubu. Můžeme toho dosáhnout preparací infikovaného dentinu, použitím vyšší koncentrace chlornanu sodného po delší dobu nebo jeho aktivací. Všechny tyto kroky vedou buď k poškození apikální papily, nebo poškození extracelulární matrix dentinu, což má za následek snížení úspěšnosti rematurogeneze.
Negativní působení chlornanu sodného na apikální papilu a Hertwigovu epiteliální pochvu lze zmírnit zkrácením pracovní délky vyplachovací kanyly a aktivační koncovky. Při využití endodontických kanyl s otevřeným zakončením (angl. open-ended) je maximální možný dosah výplachu 3 mm od konce kanyly (7, 8). U pasivní aktivace ultrazvukem (angl. passive ultrasonic irrigation, PUI) neexistuje konsenzus ohledně umístění hrotu aktivační koncovky. Podstatná část studií zmiňuje umístění koncovky 1 mm od foramen apicale (9). Nicméně při využití PUI je zvýšené riziko přetlačení chlornanu do periapikální oblasti (10). Z tohoto hlediska je zkrácení pracovní délky o 3 mm více než dostatečné.
Negativní působení chlornanu sodného na povrchu dentinu lze zvrátit následnou expozicí 17% EDTA. Bylo prokázáno, že následný výplach 17% EDTA zlepšuje adherenci a přežití kmenových buněk zubní dřeně na takto upraveném dentinu.
Je ale vhodné vyzdvihnout, že úspěch maturogeneze je s velkou pravděpodobností vázán spíše na stav Hertwigovy epiteliální pochvy než na úroveň bakteriální infekce (6, 11). Na zvířecím modelu bylo prokázáno, že přírůstek mineralizované tkáně je velmi podobný, a to jak pro případ sterilního, tak „dezinfikovaného“ kořenového systému (12).
I přes původní trauma, zánětlivé komplikace a opakovanou traumatizaci apikální papily nedošlo k destrukci Hertwigovy epiteliální pochvy a pravděpodobně vzhledem k velikosti apozici mineralizované tkáně se zachovala i apikální část radikulární dřeně. S velkou pravděpodobností v tomto případě hrál roli velmi časný vývojový stupeň vývoje kořene, jenž se dá zařadit do 2. třídy dle Cvekovy klasifikace (13). Velikost kontaktu radikulární dřeně a periapikální oblasti zajišťuje velmi bohaté cévní zásobení, které je schopno zachovat vitalitu části dřeně i při bakteriální infekci. Chan et al. ve své retrospektivní studii zjistili pozitivní vztah mezi ranými stadii vývoje kořene a velikostí zisku mineralizované tkáně při ošetření maturogenezí (14).
Dalším faktorem je vysoká odolnost apikální papily jako takové, která je schopna přežít navzdory početnému zánětlivému infiltrátu (15). Z toho můžeme vyvodit, že v raných fázích vývoje kořene je možná vyšší úspěšnost ošetření maturogenezí, alespoň co se týká apozice mineralizovaných tkání.
Posledním faktorem, který mohl v našem případě hrát pozitivní roli, byla (paradoxně) dislokace kalciumsilikátové zátky více apikálně. Tím došlo ke zmenšení celkového objemu defektu, kde bylo požadováno dosažení regenerace. V regenerativní medicíně a i regenerativní endodoncii se zmiňuje pojem „kritická velikost defektu“ (angl. critical size of the defect), tj. maximální velikost defektu, u kterého je možné dosáhnout regenerace (16). Pokud je defekt větší než kritická velikost, dochází pouze k částečné regeneraci. Je možné, že ono „propadnutí“ kalciumsilikátové zátky zmenšilo celkový objem defektu pod kritickou mez. Pro regenerativní endodoncii však nebyla velikost kritického defektu stanovena (17).
Závěr
V současné době není k dispozici přesně dané indikační spektrum, jež by určovalo, v jakých případech je vhodné se přiklonit k maturogenezi a v kterých případech se naopak přiklonit k ošetření apikální zátkou s kalciumsilikátovým cementem při ošetřování stálých zubů s nedokončeným vývojem a nekrotickou dření. U masivně infikovaného kořenového kanálku se budeme spíše přiklánět k zaplnění kořenového kanálku kalciumsilikátovým cementem nebo k využití koncentrovaného chlornanu sodného s prolongovaným použitím 17% EDTA v rámci maturogeneze. K maturogenezi se budeme spíše přiklánět v raných stadiích vývoje kořene, kde pravděpodobnou hranicí bude 3. vývojové stadium dle Cveka.
Rematurogeneze se jeví jako vhodný způsob ošetření selhavší maturogeneze, pokud je možné napravit předchozí chyby ošetření. Extrakci zubu se snažíme při ošetřování stálých zubů s nedokončeným vývojem a nekrotickou dření vyvarovat, a to zvláště ve frontálním úseku chrupu.
Obrazová dokumentace
Literatura
1. Andreasen JO, Farik B, Munksgaard EC. Long-term calcium hydroxide as a root canal dressing may increase risk of root fracture. Dent Traumatol, 2002, 18(3): 134 – 137.
2. Ree MH, Schwartz RS. Long-term success of nonvital, immature permanent incisors treated with a mineral trioxide aggregate plug and adhesive restorations: a case series from a private endodontic practice. J Endod, 2017, 43(8): 1370 – 1377.
3. Žižka R, Šedý J, Škrdlant J, Němcová N. Maturogeneze. Část 1. Úvod, anatomie, kmenové buňky, tkáňové faktory, vnitřní matrice. Čes Stomat, 2016, 116(1): 20 – 26.
4. Žižka R, Šedý J, Škrdlant J, Němcová N, Buchta T. Maturogeneze. Část 3. Klinický protokol. Prakt zub lék, 2016, 64(3): 39 – 45.
5. Žižka R, Škrdlant J, Míšová E. Maturogeneze. LKS, 2015, 25(11):220 – 228.
6. Žizka R, Buchta T, Voborná I, Harvan L, Šedý J. Root maturation in teeth treated by unsuccessful revitalization: 2 case reports. J Endod, 2016, 42(5): 724 – 729.
7. Park E, Shen Y, Haapasalo M. Irrigation of the apical root canal. Endododontic Topics, 2012, 27(1): 54 – 73.
8. Boutsioukis C, Lambrianidis T, Verhaagen B, Versluis M, Kastrinakis E, Wesselink PR, et al. The effect of needle-insertion depth on the irrigant flow in the root canal: evaluation using an unsteady computational fluid dynamics model. J Endod, 2010, 36(10): 1664 – 1668.
9. van der Sluis LW, Shemesh H, Wu MK, Wesselink PR. An evaluation of the influence of passive ultrasonic irrigation on the seal of root canal fillings. Int Endod J, 2007, 40(5): 356 – 361.
10. Tasdemir T, Er K, Celik D, Yildirim T. Effect of passive ultrasonic irrigation on apical extrusion of irrigating solution. Eur J Dent, 2008, 2(3): 198 – 203.
11. Chueh LH, Ho YC, Kuo TC, Lai WH, Chen YH, Chiang CP. Regenerative endodontic treatment for necrotic immature permanent teeth. J Endod, 2009, 35(2): 160 – 164.
12. Khademi AA, Dianat O, Mahjour F, Razavi SM, Younessian F. Outcomes of revascularization treatment in immature dog’s teeth. Dent Traumatol, 2014, 30(5): 374 – 379.
13. Cvek M. Prognosis of luxated non-vital maxillary incisors treated with calcium hydroxide and filled with gutta-percha. A retrospective clinical study. Endod Dent Traumatol, 1992, 8(2): 45 – 55.
14. Chan EK, Desmeules M, Cielecki M, Dabbagh B, Ferraz Dos Santos B. Longitudinal cohort study of regenerative endodontic treatment for immature necrotic permanent teeth. J Endod, 2017, 43(3): 395 – 400.
15. Chrepa V, Pitcher B, Henry MA, Diogenes A. Survival of the apical papilla and its resident stem cells in a case of advanced pulpal necrosis and apical periodontitis. J Endod, 2017, 43(4): 561 – 567.
16. Huang G, Al-Habib M, Gauthier P. Challenges of stem cell-based pulp and dentin regeneration: a clinical perspective. Endodontic Topics, 2013, 28(1): 51 – 60.
17. Huang GT, Garcia-Godoy F. Missing concepts in de novo pulp regeneration. J Dent Res, 2014, 93(8): 717 – 724.
11. 5. 2018
Print: LKS. 2018; 28(5): 108 – 113
Autoři:
Fotografie
- Radovan Žižka
Rubrika:
Téma: