Extrakce zubů u pacientů užívajících antiresorpční a antiangiogenní léčbu
Přehledové sdělení s kazuistikou
Souhrn: Pacientů, kteří užívají různá antiresorpční či antiangiogenní léčiva, přibývá. Extrakce zubů je v zubním lékařství jedním z nejčastějších výkonů, který je však u těchto pacientů rizikem pro rozvoj osteonekrózy. Text nabízí přehled aktuálních postojů k ošetřování pacientů s takto kompromitovaným hojením a představuje návod ke zjednodušené diagnostické rozvaze při plánování invazivních chirurgických výkonů. Šetrná extrakce se zapojením různých profylaktických opatření je předpokladem pro snížení rizika rozvoje lékově indukované osteonekrózy čelistí na minimum.
Klíčová slova: extrakce zubů, orální chirurgie, antiresorpční, antiangiogenní léčba, bisfosfonáty, MRONJ
Tooth extraction in patients on antiresorptive and anti- angiogenic therapy
Review article with case report
Summary: The number of patients on antiresorptive or anti-angiogenic therapy rapidly rises. Tooth extraction is one of the most frequent dental treatments. Yet it presents a risk factor for development of medication-related osteonecrosis of jaws (MRONJ). This text offers an overview of current approaches when treating patients with compromised healing. The article also presents simplified diagnostic criteria for treatment planning and simplified guideline for surgical intervention in MRONJ patients. A plethora of prophylactic precautions successfully minimizes the risk of osteonecrosis development.
Key words: tooth extraction, oral surgery, antiresorptive, anti- angiogenic, bisphosphonates, MRONJ
Úvod
Bisfosfonáty jsou již mnoho let léky volby při léčbě osteoporózy a některých malignit. Tlumí resorpci kosti a spolu s některými monoklonálními protilátkami patří do skupiny antiresorpčních léčiv. V onkologické terapii je využíváno také antiangiogenních látek omezujících vaskularizaci tkáně. Antiresorpční a antiangiogenní léčiva byla identifikována jako eti opatologická agens lékové osteonekrózy čelistí (medication-related osteonecrosis of jaws – MRONJ).
Indikací pro použití těchto látek přibývá stejně jako pacientů vyžadujících tuto léčbu a také nových léků s potenciálem indukovat rozvoj osteonekrózy. Zubní lékaři se v ordinacích stále častěji setkávají s pacienty se zvýšeným rizikem MRONJ. Invazivní stomatologické výkony zasahující do integrity tvrdých i měkkých tkání jsou jedním ze spouštěcích faktorů osteonek rózy. Pacienti se zvýšeným rizikem MRONJ proto vyžadují zvláštní přístup při plánování a provádění takovýchto výkonů. Nejběžnějším chirurgickým výkonem v dutině ústní je extrakce zubu.
Osteonekróza čelistí
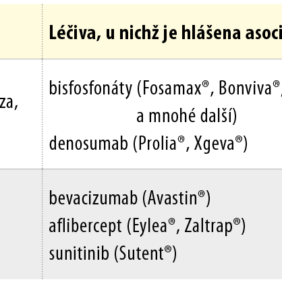
Osteonekróza čelistí je patologický stav charakterizovaný různě rozsáhlou nekrózou čelistních kostí, kdy část nevitální kosti komunikuje slizniční ranou s dutinou ústní nebo extraorálně (1). Mezi další klinické projevy patří bolest, intra- nebo extraorální píštěl, oroantrální komunikace, pyorrhea, spontánní kostní sekvestr a patologická zlomenina (2, 3). Příčiny vzniku těchto lézí jsou nejčastěji iatrogenní (radioterapie, farmakoterapie), traumatické nebo infekční. Osteonekróza čelistí vznikající jako nežádoucí účinek systémové farmakoterapie (MRONJ) je závažnou komplikací postihující pacienty s určitým typem antiresorpční nebo antiangiogenní léčby (tab. I).
Pro diagnózu MRONJ je nutno splnit následující tři kritéria (4):
1. antiresorpční nebo antiangiogenní léčba v anamnéze,
2. klinická přítomnost obnažené kosti nebo píštěle alespoň 8 týdnů (vhodné doplnit radiografií),
3. absence předchozí radioterapie hlavy a krku.
Antiresorpční léčba
Antiresorpční léčba bývá u pacientů indikována u dvou typů onemocnění. Prvním je osteoporóza, druhým pak maligní tumory. Osteoporóza postihuje častěji ženy, což také vede k vyšší prevalenci MRONJ u žen (4). Cílem aplikace antiresorpčních léčiv je snížení aktivity osteoklastů, tedy zmírnění resorpčních pochodů v kosti, a tím zabránění úbytku kostní hmoty. V případě malignit je pak jejich užívání spojeno také s inhibicí tumorózních buněk, omezením perfuze a tím metabolismu nádorové tkáně.
Antiresorpční léčba využívá různých strategií. Dusíkaté bisfosfonáty (BF) deregulují buněčné pochody v osteoklastech, což vede k útlumu jejich diferenciace až k apoptóze (5). Současně blokují aktivaci osteoklastů systémem RANK/RANKL (receptor aktivující nukleární faktor κB/ligand pro receptor aktivující nukleární faktor κB) vazbou na buněčný receptor, omezují angiogenezi kompetitivní inhibicí cévního-endoteliálního růstového faktoru (VEGF), jsou keratotoxické, což přispívá k rozpadu epitelu nad nekrotickým ložiskem a omezení epitelizace ran, a poškozují makrofágy (6). Vysoká afinita dusíkatých BF k osteoblastům a osteoklastům vede k jejich akumulaci v kosti a prakticky doživotnímu ireverzibilnímu účinku (7).
Mezi antiresorpční látky patří také monoklonální protilátka (monoclonal antibody – MAB) denosumab, využívaná v léčbě zejména post-menopauzální osteoporózy a maligních tumorů. Denosumab vazbou na RANKL zabraňuje aktivaci RANK na osteoklastech a jejich prekurzorech a tím tlumí resorpci (8). Nástup účinků po jeho podání je rychlý a po vysazení léku opět rychle odeznívají. Po 2 měsících od poslední aplikace je léčivo z 80 % rozloženo, biologický poločas je asi 26 dní, k jeho akumulaci v kosti nedochází (9).
Antiangiogenní léčba
Antiangiogenní léčba bývá součástí onkologické terapie. Některé léky s tímto účinkem prokázaly vliv na rozvoj MRONJ. Patří mezi ně bevacizumab, aflibercept a sunitinib (10). Tyto látky spojuje schopnost blokovat VEGF, což vede k potlačení vaskularizace. Sunitinib navíc blokuje i buněčný receptor pro destičkový růstový faktor (PDGF) (11) a inhibuje diferenciaci celé monocyto-makrofágové linie, jejíž součástí jsou i osteoklasty (6).
Další léčiva jako odanacatib (inhibitor katepsinu K tlumící kostní resorpci), everolimus (imunosupresivum využívané při transplantacích a léčbě malignit) nebo sorafenib jsou rovněž podezřelá z vlivu na rozvoj MRONJ (12).
Prevence před zahájením léčby
Opatření před zahájením léčby zahrnují omezení známých rizikových faktorů, ošetření aktuálně přítomných patologií (sanace chrupu, extrakce aj.) a také poskytnutí informací o rizicích a jejich prevenci pacientovi, jeho motivaci a instruktáž. Autodiagnostika, tedy schopnost pacienta rozpoznat počínající patologii, je účinným nástrojem předcházení rozsáhlých postižení, stejně jako důraz na pravidelné prohlídky během léčby.
Výkony kontraindikované před zahájením onkologické léčby (u léčby osteoporózy vzniká riziko výrazně později) jsou implantace a augmentace. Vytvářejí významné nové riziko komplikací v budoucnu, které zpravidla převyšuje jejich přínos (12).
Další variantou primární prevence je zvážení alternativního léčiva, které namísto útlumu resorpce kosti podporuje její apozici. Takto působí například rekombinantní analogon parathormonu teriparatid (8).
Prevence během léčby
U pacientů s již probíhající antiresorpční nebo antiangiogenní léčbou tvoří soubor preventivních opatření příprava před výkonem, výkon samotný i sledování po něm.
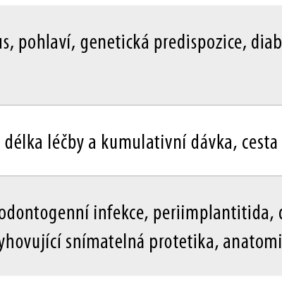
Primární prevencí je opět omezení rizikových faktorů (tab. II) (2, 12 – 14), včasná sanace chrupu a poskytnutí informací. Systémové rizikové faktory nebo ty vztažené k léčivu zpravidla není možné z pozice stomatologa ovlivnit. Předejít MRONJ tedy můžeme zejména ovlivněním lokálních faktorů.
Specifická anamnéza u pacientů s rizikem MRONJ
Onemocnění
Léčba osteoporózy vyžaduje výrazně menší dávky antiresorpčních léčiv, často stačí perorální příjem, než je tomu u maligních nádorových onemocnění. Nejčastěji jde o mnohočetný myelom, velkobuněčný kostní nádor a kostní metastázy karcinomu prostaty, prsu a štítné žlázy. U těch se aplikují vyšší dávky spíše intravenózně, což vede k rychlejšímu a závažnějšímu ovlivnění kostního metabolismu.
Typ léčiva
Dusíkaté bisfosfonáty mají výrazně větší afinitu ke kostním buňkám než starší nedusíkaté látky a v kosti se akumulují. BF se mezi sebou liší také rychlostí nástupu účinku nebo délkou biologického poločasu. Obecná doporučení je proto třeba konfrontovat s konkrétním použitým léčivem. Při dlouholeté léčbě je pak nezřídka využito postupně nebo i současně více rizikových léčiv z různých skupin, na což je nutno v anamnéze klást důraz. Oproti tomu u monoklonálních protilátek a cytostatik není akumulace v kostech prokázána.
Délka léčby
Nástup žádoucích i nežádoucích účinků antiresorpčních či antiangiogenních léčiv trvá různě dlouho. U denosumabu a bevacizumabu obecně týdny, u BF spíše týdny až měsíce v závislosti na cestě podání. V případě užívání malých dávek perorálních BF pro léčbu osteoporózy a absence dalších rizikových faktorů lze považovat riziko rozvoje MRONJ za nízké, ne však nulové, při trvání léčby do 3 let (15), podle jiných autorů až do 4 let (14). Ve všech ostatních případech nehraje délka užívání zásadní roli a preventivní opatření jsou na místě vždy.
Cesta podání
U perorálního užívání léčiv je výrazně nižší biologická dostupnost a účinek nastupuje později než při aplikaci intravenózní. V případě příjmu BF v perorální formě v indikaci léčby osteoporózy po dobu kratší než 4 roky je riziko nízké (4) a je tedy možno postupovat bez zvláštních opatření a pacienta ošetřovat běžným způsobem. To neplatí pro vysoké dávky podávané pacientům s onkologickou diagnózou intravenózně. Pro doplnění, denosumab je aplikován subkutánně, bevacizumab a aflibercept intravenózně, sunitinib perorálně. Cesta podání u nich nemá na rozvoj MRONJ vliv.
Poslední užití, vysazení
V případě bisfosfonátů bylo v mnoha studiích potvrzeno, že doba od posledního užití nemá pro prevenci MRONJ zásadní vliv (16). I roky po ukončení léčby je efekt v kosti vázaných BF významný a nutnost profylaktických opatření trvá prakticky doživotně. Benefity antiresorpční léčby však převyšují riziko MRONJ. Jakékoli vysazování se tedy i přes existenci dobře navržených schémat „lékových prázdnin“ (drug holiday) nedoporučuje (17, 18). Přesto je vhodné načasovat výkon při nepřerušeném příjmu BF asi do jedné čtvrtiny intervalu mezi poslední a následující dávkou, kdy je plazmatická hladina léčiva již poměrně nízká a po dobu hojení operačního defektu její úroveň nadále klesá (12).
Jak již bylo zmíněno, doba uplynulá od vysazení léčiva hraje roli zejména u monoklonálních protilátek. V případě denosumabu se resorpce kosti normalizuje 6 měsíců po poslední injekci, tehdy pacient s diagnózou osteoporózy dostává zpravidla další dávku. Ale již po 2 měsících je jeho účinek minimální. Vzhledem k žádoucí nepřítomnosti léčiva v plazmě nejen během výkonu, ale zvláště během tvorby nové kosti, se doporučuje provést plánovanou extrakci 2 měsíce po poslední a tedy 4 měsíce před následující dávkou – bez nutnosti přerušení léčby (5).
V případě bevacizumabu je doporučeno provést výkon 6 – 7 týdnů po poslední a 4 – 6 týdnů před následující dávkou (12), u sunitinibu a afliberceptu pak v půli intervalu mezi jednotlivými léčebnými cykly.
Vhodná může být také náhrada BF při léčbě osteoporózy anabolickým teriparatidem, který stimuluje kostní resorpci bez vlivu na hojení (19). Sledování markerů kostní obměny, coby nástroje pro zhodnocení rizika MRONJ u konkrétního pacienta, je považováno za neprůkazné a není doporučeno (8).
Vždy je nezbytné přihlédnout k dalším onemocněním (např. imunopatologie, diabetes mellitus, anemie) a lékům (např. imunosupresiva, cytostatika), které mohou přispět k nižší tendenci k hojení ran (4).
Kontrolní body
Rozvaha během plánování invazivního výkonu u pacienta s rizikem MRONJ by tedy měla obsahovat zejména tyto otázky:
- Z jakého důvodu přijímá pacient antiresorpční či antiangiogenní léčbu? Osteoporóza nebo malignita?
- Jaký lék pacient užívá nyní a jaké léky užíval dříve? Jde o BF nebo jiný lék?
- Jak dlouho a jakou cestou pacient lék užívá?
- Jak dlouhá doba uplynula od posledního užití?
- Jaký bude rozsah operačního výkonu?
- Jaké další léky pacient užívá, jaká má další onemocnění, je alergický, kouří?
Poučení pacienta o riziku
Součástí úspěšného léčebného plánu je důkladné poučení pacienta o možných komplikacích výkonu souvisejících s užívanou antiresorpční či antiangiogenní léčbou, včetně návrhu alternativních způsobů léčby.
Extrakce zubu
Extrakce zubu je spouštěcím faktorem 50 – 60 % případů MRONJ. V některých případech lze i k pacientovi s antiresorpční léčbou přistupovat bez omezení (viz výše). V ostatních situacích je standardem profylaxe širokospektrým antibiotikem pro vytvoření chráněného koagula (20). Infekce v ráně znesnadňuje hojení pooperačního defektu. Je proto na místě udělat vše pro to, aby inhibované osteoklasty a kompromitovaný imunitní systém měly co nejméně úkolů.
Volba antibiotika se řídí dalšími onemocněními, farmakologickou a alergologickou anamnézou. Dávkování odpovídá běžnému profylaktickému režimu (např. amoxicilin/klavulanát 1 g po 12 h) započatému dostatečně dlouho předem pro dosažení maximální plazmatické koncentrace během výkonu a vytvoření chráněného krevního koagula – v případě per os podání kombinace amoxicilin/klavulanát stačí k dosažení maximální plazmatické koncentrace 1 – 2 hodiny (21). Někteří autoři však doporučují zahájit antibiotickou profylaxi už 1 nebo 2 dny před výkonem (15, 20).
Chirurgický výkon
Chirurgický výkon vyžaduje co nejšetrnější přístup, tvorbu řezných chirurgických ran a umožnění optimálního hojení, ideálně per primam intentionem. Roztržení či zhmoždění měkkých nebo tvrdých tkání zvyšuje riziko rozvoje osteonekrózy. Tkáň disponuje omezenou perfuzí, slabou tendencí k hojení, dysfunkcí resorpce i depozice kosti.
Extrakci je doporučeno zahájit i ukončit výplachem 0,2% chlorhexidinem (CHX). Po anestezii oblasti lokálním anestetikem následuje vždy odklopení mukoperiostálního laloku podle předpokládaného objemu kosti na konci výkonu. Takový lalok musí umožnit přístup, přehled, zvláště pak hermetickou suturu po často značné egalizaci alveolárního výběžku. Připojenou gingivu po celém obvodu zubu oddělujeme ostře protětím skalpelem pro vytvoření ostrých chirurgických ran nezbytných k primárnímu hojení, zhmožděný okraj laloku nebo epitel na styku laloků naopak hojení prodlužuje. Při riziku komprese nebo fraktury alveolární kosti ihned zub dekapitujeme, případně separujeme kořeny, či snášíme okolní kost – zub vybavíme s minimálním zhmožděním kosti. Vzhledem k léky omezené perfuzi a kostní remodelaci je vhodné snést veškeré kostěné lamely tenčí než 2 mm, což může vést k rozsáhlé egalizaci a výrazné změně ve tvaru defektu. K tomu je vhodné přihlížet už při návrhu laloku. Výkon je ukončen toaletou rány (např. lokálním antibiotikem), pokud možno primární suturou a CHX výplachem. To vše ve snaze předejít infekci rány jako jednomu z etiopatogenetických činitelů rozvoje MRONJ (17, 22, 23).
Nedávno publikovaná studie vyhodnotila 2458 extrakcí provedených u 1175 pacientů s rizikem MRONJ. V 1,7 % případů se rozvinula postextrakční léky indukovaná osteonekróza. Žádná se nerozvinula při dodržení výše zmíněných postupů (17).
Na našem pracovišti doplňujeme chirurgický výkon, obzvláště při vysoké míře rizika vzniku MRONJ, o aplikaci autologního destičkového koncentrátu do extrakčního lůžka před závěrečnou suturou. Používáme fibrin bohatý na trombocyty (platelet-rich fibrin – PRF) připravený standardním způsobem (24). Aplikace destičkového koncentrátu dle studií snižuje incidenci MRONJ po extrakci zubu, ačkoli prokázaný rozdíl není statisticky významný (25).
Pooperační péče
Pro podporu hojení rány, minimálně týden (podle některých autorů až do úplného zhojení) pacient provádí několikrát denně antiseptické výplachy (např. 0,12% chlorhexidin, nebo 3% H2O2), nebo aplikuje CHX ve formě 1% gelu přímo na oblast rány. Rovněž profylaktické působení antibiotika je důležité i po operaci. Dle Italské společnosti pro maxilofaciální chirurgii (SICMF) je vhodné ukončit antibiotickou profylaxi 6 dní po výkonu, dle jiných až po úplném zhojení. Léčbu je vhodné doplnit probiotikem. Doporučuje se také biostimulace laserem či rekonstituční doplněk stravy (15).
Sledování a farmakovigilance
Kolem 88 % léky indukovaných osteonekróz se projeví do 8 týdnů od výkonu. Je proto doporučeno kontrolovat rizikové pacienty po extrakci co 14 dní po dobu 8 týdnů (17), jako součást sekundární prevence.
Při jistotě zhojení rány ukončujeme profylaxi antibiotikem a antiseptickými výplachy. V případě rozvoje MRONJ odesíláme pacienta na specializované pracoviště. Výskyt nežádoucího účinku léku je vhodné ohlásit na SÚKL, registrovaní lékaři podávají hlášení do Registru bisfosfonátových osteonekróz na webové adrese https://registrbo.fno.cz (26).
Kazuistika
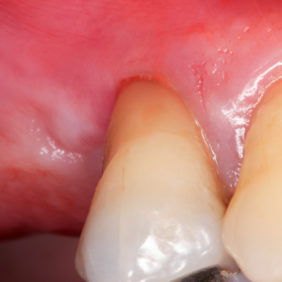
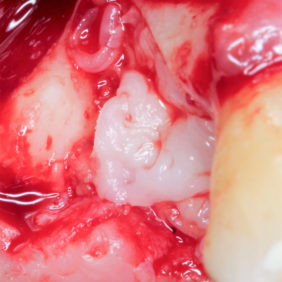
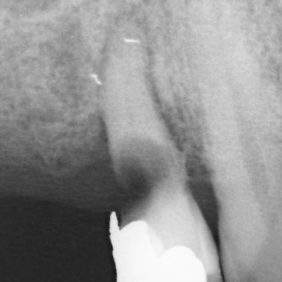
Šedesátiletá pacientka byla odeslána na naše oddělení svým praktickým zubním lékařem k extrakci zubu 14 (obr. 1) pro caries ad pulpam penetrans na distální straně zubu. V anamnéze pacientky dominoval mnohočetný myelom a revmatoidní artritida. Pacientka přijímá již dva roky intravenózně aminobisfosfonát zoledronát (Zometa®), poslední dávka byla aplikována před dvěma měsíci. Dále užívá glukokortikoid metylprednisolon (Medrol®) a imunosupresivum leflunomid (Arava®). Ostatní anamnestické údaje byly nevýznamné. Intravenózní příjem bisfosfonátu spolu s imunosupresí metylprednisolonem a leflunomidem jsou významnými rizikovými faktory pro vznik osteonekrózy čelistí.
Vzhledem k riziku rozvoje MRONJ bylo rozhodnuto o extrakci s maximálně profylaktickým přístupem. Dva dny před výkonem začala pacientka užívat širokospektré antibiotikum (amoxicilin/klavulanát 1 g po 12 h) spolu s probiotikem. Žádné léčivo vysazeno nebylo.
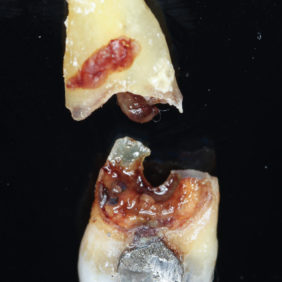
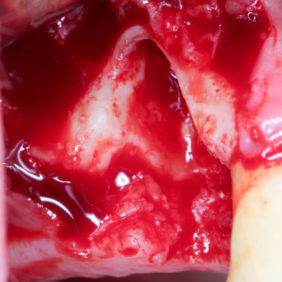
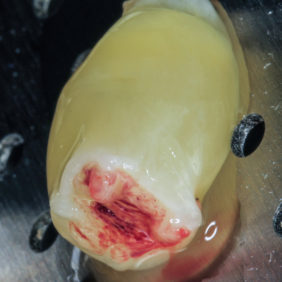
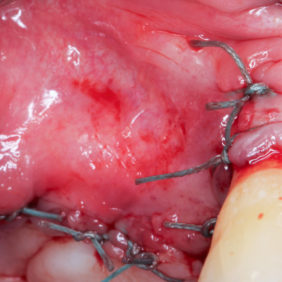
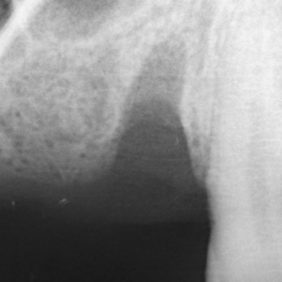
V lokální anestezii 2 ml Supracainu® 4% bylo provedeno protětí dento-gingiválního uzávěru skalpelem, následně byl preparován hokejkový mukoperiostální lalok a zub byl subluxován pomocí Beinovy páky. Vinou rozsáhlé kariézní destrukce v oblasti krčku zubu (obr. 2) byl zub dekapitován, snesena část bukální kostní lamely a šetrně vybaven kořen zubu. Po důkladné exkochleaci zubního lůžka byla provedena rozsáhlá egalizace ostrých okrajů extrakční rány včetně části bukální stěny (obr. 3). Ponechání tenké kosti o tloušťce menší než 2 mm bychom považovali vzhledem k omezené perfuzi a kostní resorpci za rizikové. Po toaletě rány bylo extrakční lůžko vyplněno zátkou z autologního destičkového koncentrátu (obr. 4), (obr. 5), fibrinem bohatým na trombocyty (platelet-rich fibrin – PRF) zhotoveným standardním způsobem (24) z 10 ml autologní krve odebrané pacientce bezprostředně před výkonem. Extrakce byla zakončena uzavřením laloku jednoduchými nevstřebatelnými stehy (obr. 6).
V pooperační péči bylo pacientce zdůrazněno šetřené chování k extrakční ráně. Dále byla instruována k výplachům 3% H2O2 3x denně a následnému potření rány 1% chlorhexidinovým gelem. V užívání předepsaného širokospektrého antibiotika nadále pokračovala až do vytažení stehů. Ke kontrolám byla zvána každých 7 dní.
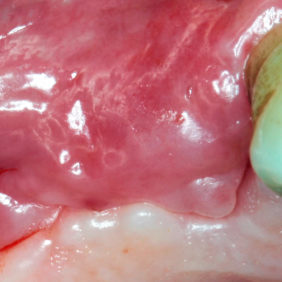
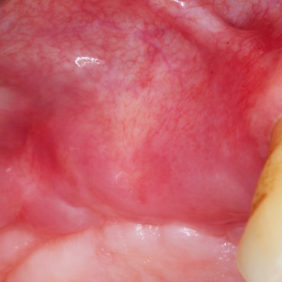
Již po 2 týdnech byla reepitelizace okrajů rány kompletní (obr. 7), stehy vyjmuty a profylaktická opatření ukončena. Po 3 týdnech pak byla rána prakticky zhojena (obr. 8). Dále je pacientka sledována vždy po 1 měsíci. Dokumentaci doplňují intraorální rentgenové snímky před výkonem (obr. 9) a 3 týdny po výkonu (obr. 10).
Závěr
Maximum plánovaných invazivních výkonů by mělo být provedeno před zahájením antiresorpční či antiangiogenní léčby. Neléčená apikální periodontitida může například sama o sobě být příčinou rozvoje MRONJ, nebo dokonce již jejím projevem (27). Proto by ani ošetření chronických stavů, ač asymptomatických, nemělo být odkládáno. V případě dosud nediagnostikované MRONJ s neexponovanou lézí pak dodržení výše zmíněných postupů může vést k včasné diagnostice – po odklopení mukoperiostálního laloku je nekrotická kost často vizuálně rozpoznatelná.
Popsané zásady lze aplikovat i při jiných invazivních chirurgických výkonech, jako je otevřená kyretáž, mukogingivální nebo periapikální chirurgie. Doporučené koncepty však nemají jednoznačné hranice, zodpovědnost zůstává na ošetřujícím lékaři a jeho individuálním posouzení pacienta a všech faktorů modulujících riziko vzniku MRONJ. Konečný zvolený postup pak vychází z komunikace mezi zubním lékařem, ošetřujícím všeobecným lékařem a pacientem.
Práce vznikla v rámci projektu NV16 – 28462A a specifického výzkumu MUNI/A/1008/2017.
Použité zkratky
AAOMS – American Association of Oral and Maxillofacial Surgeons
BF – bisfosfonáty
CHX – chlorhexidin diglukonát
MAB – monoclonal antibody, monoklonální protilátka
MRONJ – medication-related osteonecrosis of jaws, dříve používaná zkratka BRONJ postihovala pouze vliv bisfosfonátů, od odhalení potenciálu indukovat nekrózu i u jiných léčiv se užívá zkratky MRONJ, nebo pouze ONJ, vzácněji také ARONJ (antiresorptive agent-induced osteonecrosis of jaws), což ale opomíjí antiangiogenní léčiva
PDGF – platelet-derived growth factor
PRF – platelet-rich fibrin
RANK – receptor aktivující nukleární faktor κB
RANKL – ligand pro receptor aktivující nukleární faktor κB
SÚKL – Státní ústav pro kontrolu léčiv
VEGF – vascular-endothelial growth factor
Obrazová dokumentace
Literatura
1. Peřina V. Osteonekróza čelisti – komplikace komplexní onkologické terapie. Klinická onkologie, 2015, 28(Suppl. 1): S55.
2. Filleul O, Crompot E, Saussez S. Bisphosphonate-induced osteonecrosis of the jaw: a review of 2,400 patient cases. Journal Of Cancer Research And Clinical Oncology, 2010, 136(8): 1117 – 1124.
3. Ruggiero SL, Dodson TB, Assael LA, Landesberg R, Marx RE, Mehrotra B. American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaw – 2009 update. Australian Endodontic Journal, 2009, 35(3): 119 – 130.
4. Ruggiero SL, Dodson TB, Fantasia J, Goodday R, Aghaloo T, Mehrotra B, et al. American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw – 2014 update. Journal Of Oral And Maxillofacial Surgery, 2014, 72(10): 1938 – 1956.
5. Damm DD, Jones DM. Bisphosphonate-related osteonecrosis of the jaws: a potential alternative to drug holidays. General Dentistry, 2013, 61(5), 33 – 38.
6. Pazianas M. Osteonecrosis of the Jaw and the Role of Macrophages. J Natl Cancer Inst, 2011, 103(3): 232 – 240.
7. Jones AC, Hellstein J. Recommendations questioned. 2012, 732 – 4.
8. Hellstein JW, Adler RA, Edwards B, Jacobsen PL, Kalmar JR, Koka S, et al. Managing the care of patients receiving antiresorptive therapy for prevention and treatment of osteoporosis: Recommendations from the American Dental Association Council on Scientific Affairs. American Dental Association [Internet]. 2011, 142(11). Available from: http://search.ebscohost.com/login.aspx?direct=true&db=mdc&AN=22041409.
9. Charopoulos I, Orme S, Giannoudis PV. The role and efficacy of denosumab in the treatment of osteoporosis: an update. Expert Opinion On Drug Safety, 2011, 10(2): 205 – 217.
10. Guarneri V, Miles D, Robert N, Diéras V, Glaspy J, Smith I, et al. Bevacizumab and osteonecrosis of the jaw: incidence and association with bisphosphonate therapy in three large prospective trials in advanced breast cancer. Breast Cancer Research And Treatment, 2010, 122(1): 181 – 188.
11. Mendel DB, Laird AD, Xin X, Louie SG, Christensen JG, Li G, et al. In vivo antitumor activity of SU11248, a novel tyrosine kinase inhibitor targeting vascular endothelial growth factor and platelet-derived growth factor receptors: determination of a pharmacokinetic/pharmacodynamic relationship. Clinical Cancer Research, 2003, 9(1): 327 – 337.
12. Campisi G. Gestione odontoiatrica del paziente a rischio di ONJ. National conference on dental management of patients with risk of medication-related osteonecrosis of jaws, Italian Society for Maxillofacial Surgery and Italian Society for Oral Medicine and Pathology, Nuoro: Universita degli Studi di Palermo, 2017.
13. Pazianas M. Osteonecrosis of the jaw associated with antiresorptives: more evidence on the role of infection. IBMS BoneKEy, 2013, 10(11): 441.
14. Kim KM, Rhee Y, Kwon Y-D, Kwon T-G, Lee JK, Kim D-Y. Medication Related Osteonecrosis of the Jaw: 2015 Position Statement of the Korean Society for Bone and Mineral Research and the Korean Association of Oral and Maxillofacial Surgeons. Journal Of Bone Metabolism, 2015, 22(4): 151 – 165.
15. Di Fede O, Panzarella V, Campisi G. Protocollo per estrazioni dentarie e chirurgia minor in soggetti a rischio di MRONJ Palermo 2016.
16. Hauer L, Hrušák D, Hostička L, Andrle P, Jambura J, Pošta P, et al. Chirurgická terapie osteonekrózy čelistí způsobené léčivy. LKS, 2014, 24(6): 130 – 135.
17. Hasegawa T, Kawakita A, Ueda N, Funahara R, Tachibana A, Kobayashi M, et al. A multicenter retrospective study of the risk factors associated with medication-related osteonecrosis of the jaw after tooth extraction in patients receiving oral bisphosphonate therapy: can primary wound closure and a drug holiday really prevent MRONJ? Osteoporosis International, 2017, 28(8): 2465 – 2473.
18. Hauer L, Hrušák D, Jambura J, Hora M. Osteonekróza čelistí jako nežádoucí účinek léčby urologických onkologických pacientů. Česká urologie, 2013, 17(2): 88 – 99.
19. Rosa J. Teriparatid 20 µg denně v terapii osteoporózy. Farmakoterapie, 2007, 3(5): 461 – 466.
20. Montefusco V, Gay F, Spina F, Miceli R, Maniezzo M, Teresa Ambrosini M, et al. Antibiotic prophylaxis before dental procedures may reduce the incidence of osteonecrosis of the jaw in patients with multiple myeloma treated with bisphosphonates. Leukemia & Lymphoma, 2008, 49(11): 2156 – 2162.
21. Hájek P. Využití antibiotika AMOKSIKLAV v oboru ústní chirurgie a dentální implantologie. Medical tribune, 2007, 3(26): 4.
22. Ferlito S, Puzzo S, Liardo C. Preventive protocol for tooth extractions in patients treated with zoledronate: a case series. Journal Of Oral And Maxillofacial Surgery, 2011, 69(6): e1-e4.
23. Di Fede O, Panzarella V, Campisi G. Protocollo per estrazioni dentarie e chirurgia minor in soggetti a rischio di ONJ. Palermo 2016.
24. Vokurka J, Fassmann A, Izakovičová Hollá L. Deriváty krevní plazmy v zubním lékařství. LKS, 2015, 25(3): 52 – 57.
25. Del Fabbro M, Gallesio G, Mozzati M. Autologous platelet concentrates for bisphosphonate-related osteonecrosis of the jaw treatment and prevention. A systematic review of the literature. European Journal Of Cancer, 2015, 51(1): 62 – 74.
26. Uhříková T, Hodan R, Pavlíková G, Peřina V, Daněk Z, Štembírek J. Léky indukovaná osteonekróza čelistí a registr bisfosfonátových osteonekróz čelistí v České republice. LKS, 2015, 25(7 – 8): 150 – 155.
27. Otto S, Tröltzsch M, Jambrovic V, Panya S, Probst F, Ristow O, et al. Tooth extraction in patients receiving oral or intravenous bisphosphonate administration: A trigger for BRONJ development? Journal Of Cranio-Maxillo-Facial Surgery, 2015, 43(6): 847 – 854.
19. 9. 2018
Print: LKS. 2018; 28(9): 188 – 194
Autoři:
Fotografie
- Filip Hromčík
Rubrika:
Téma: