Ošetření zubu s neukončeným vývojem a dens invaginatus pomocí kalciumsilikátové zátky
Kazuistika
Souhrn: V prezentované kazuistice je popsán případ endodontického ošetření stálého zubu s neukončeným vývojem a vývojovou anomálií tvaru korunky – dens invaginatus. Je popsán postup zaplnění zubu s neukončeným vývojem a v rámci diskuze jsou vyzdviženy faktory, které ovlivňují úspěch ošetření.
Klíčová slova: zub s neukončeným vývojem, kalciumsilikátový cement, endodontické ošetření, dens invaginatus
Calcium silicate apical plug of immature tooth with dens invaginatus
Case report
Summary: In this case report the treatment of immature permanent tooth with dens invaginatus is described. The whole procedure of filling with calcium silicate cement is delianeated and factors which affect outcome are discussed.
Key words: immature tooth, calcium silicate cement, root canal treatment, dens invaginatus
Úvod
Kalciumsilikátový cement ProRoot MTA (Dentsply, Tulsa, USA) byl původně uveden na trh jako materiál pro překrytí perforací a jako retrográdní výplňový materiál [1]. Pro výbornou biokompatibilitu se jeho terapeutické využití rozšířilo i o výkony se zachováním vitality pulpy, ošetření resorpcí, výkony regenerativní endodoncie a v neposlední řadě i k zaplnění kořenových kanálků. Využití kalciumsilikátových cementů je obzvláště žádoucí v případě, kdy je obtížné vysušení kořenového kanálku (např. zub s neukončeným vývojem) a kde by konvenční plnění pomocí gutaperči a sealeru bylo velmi komplikované, nebo téměř nemožné.
I přes vynikající klinické vlastnosti kalciumsilikátových cementů mají pověst obtížně zpracovatelného materiálu, s kterým se pouze velmi obtížně manipuluje. Tato pověst je z velké části dána jinou konzistencí, která nemá v zubním lékařství obdoby a jenž klade zvýšenou náročnost nejen na zubního lékaře, ale i na asistenci.
Bylo popsáno velké množství způsobů plnění kořenových kanálků pomocí kalciumsilikátových cementů [2, 3], z nichž některé ale patří pouze do rukou zubních lékařů specializujících se na endodoncii. Cílem tohoto praktického sdělení je představit návod pro praktického zubního lékaře na zaplnění jednodušších kořenových kanálků pomocí kalciumsilikátových cementů.
Vlastní pozorování
Patnáctiletý pacient se dostavil do naší praxe se žádostí ošetřující ortodontistky o konzultaci možnosti ošetření horního levého laterálního řezáku (zub 22). Pacient udává občasnou citlivost, která s postupem času nabývá na intenzitě. Udává zvláště citlivost na skus a při palpaci vestibulárně v místě hrotu kořene zubu 22. Pacient byl celkově zdravý, neužíval trvale žádnou medikaci a neudával v anamnéze žádnou alergii.
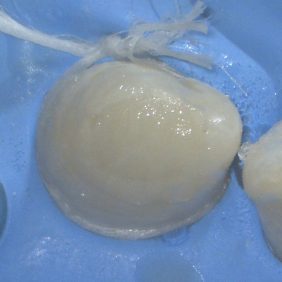
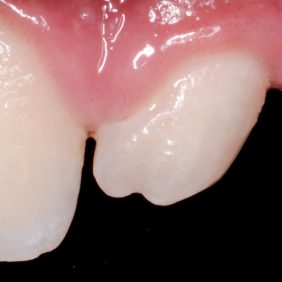
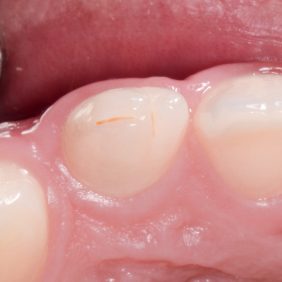
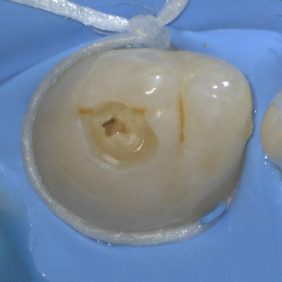
Při klinickém vyšetření nacházíme sanovaný stálý chrup s agenezí zubu 12 a zub 22 čípkovitého tvaru (obr. 1). I když byl pacient odeslán od ošetřující ortodontistky, v současné době není v plánu ortodontická terapie. Zuby horního frontálního úseku jsou poklepově nebolestivé s výjimkou zubu 22. Při palpaci pacient udává nepatrnou citlivost v místě hrotu kořene zubu 22. Parodontální sondáž dosahuje do 2 mm, bez indukovaného krvácení. Klinická korunka zubu 22 má čípkovitý tvar s výrazným vertikálním zářezem na incizi a meziodistální rýhou přítomnou na aberantním hrbolku (obr. 2).
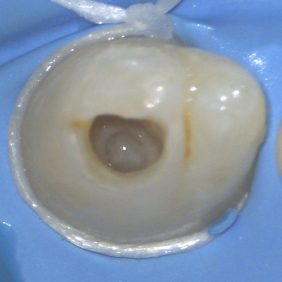
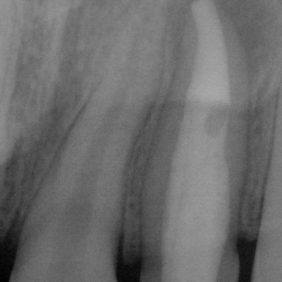
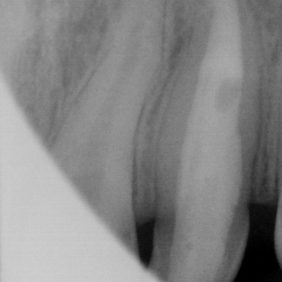
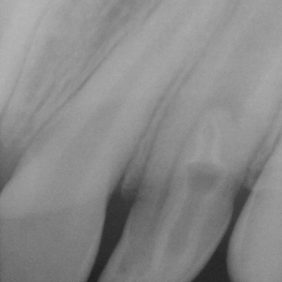
Na diagnostických snímcích (obr. 3), (obr. 4) je zřetelný periapikální nález v okolí hrotu kořene 22, který nemá ukončený vývoj, a taktéž zastínění v korunkové části, s centrálním projasněním odpovídajícím vývojové anomálii tvaru zubu, dens invaginatus. Vzhledem k faktu, že není přítomna komunikace invaginace se závěsným aparátem a taktéž apikální okraj invaginace zasahuje pod cementosklovinnou hranici, byla tato invaginace zařazena do 2. třídy dle Oehlerse [4].
Pacient s doprovodem jsou motivováni k léčbě. K extrakci zubu 22 se staví odmítavě, chtějí zub zachovat, pokud to bude možné. Po vysvětlení možností ošetření jsme přikročili k ortográdnímu endodontickému ošetření s odbroušením invaginace.
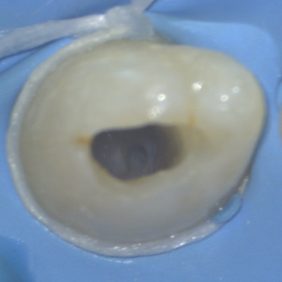
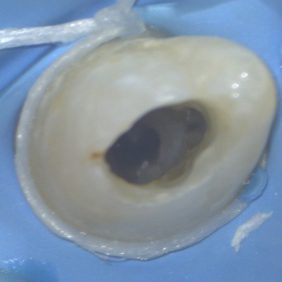
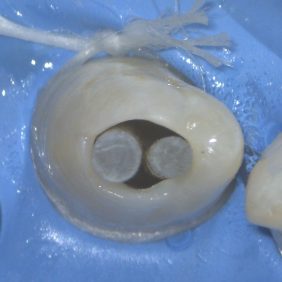
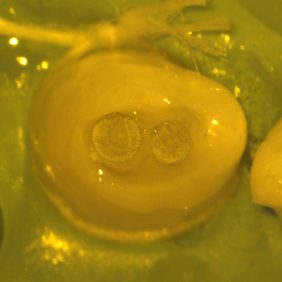
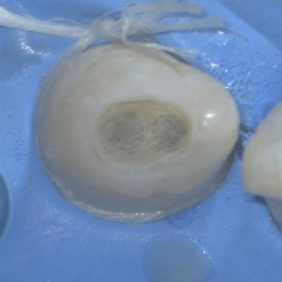
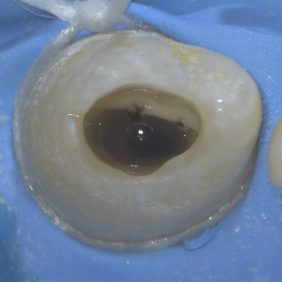
V topické anestezii 10% lidocainu (Lidocain EGIS 10%, EGIS Pharmaceuticals, Budapešť, Maďarsko) a infiltrační anestezií 4% articainem (4% Supracain, Zentiva, Praha, Česká republika) byl nasazen kofferdam. V prvotní fázi ošetření bylo provedeno odbroušení vstupu do invaginace (obr. 5). Při trepanaci cavum pulpae došlo k odtoku hnisavého exsudátu (obr. 6). Po odbroušení invaginace je viditelná komunikace s cavum pulpae (obr. 7), která byla rozšířena až do místa meziálního rohu cavum pulpae (obr. 8). Za účelem dosažení optimálního přehledu byl trepanační otvor extendován meziálně (obr. 9).
Byla stanovena pracovní délka pomocí apexlokátoru a po pasivní ultrazvukové aktivaci byl proveden závěrečný výplachový protokol, určený pro silně infikované kořenové kanálky dle České endodontické společnosti, tj. 5% chlornan sodný (10 ml), 17% ethylendiaminotetraoctová kyselina (1 minuta) a 2,5% chlornan sodný (10 ml).
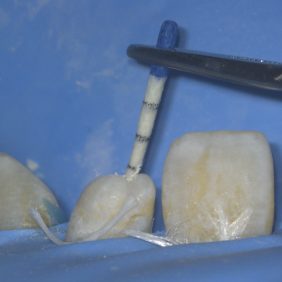
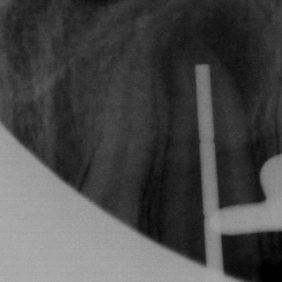
Vzhledem k nedokončenému vývoji kořene jsme přikročili k zaplnění kořenového kanálku pomocí kalciumsilikátového cementu MTA+ (Cerkamed, Nisko, Polsko). Vybrali jsme plugger takové velikosti, aby co nejvíce odpovídal velikosti foramen apicale, a vyzkoušeli jsme, zda jsme schopni jej zavést na pracovní délku zkrácenou o 0,5 mm oproti délce kořenového kanálku stanovené pomocí apexlokátoru. Následně jsme zhotovili kontrolní rentgenový snímek (obr. 10).
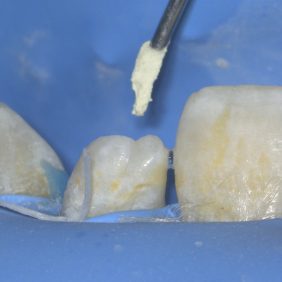
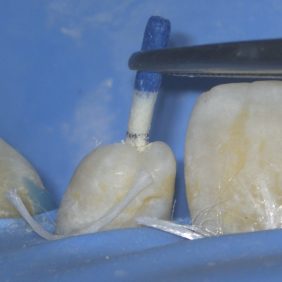
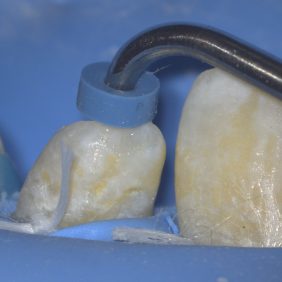
Po vysušení kořenového kanálku byl připraven kalciumsilikátový cement a na špičce pluggeru aplikován do kořenového kanálku (obr. 11). Plugger byl zaveden na předem odzkoušenou pracovní délku a kalciumsilikátový cement byl opatrně kondenzován (obr. 12). Výhodou je kondenzace materiálu pod přímou kontrolou zraku (obr. 13), i když v tomto případě je možno dosáhnout kontroly striktním dodržováním pracovní délky a taktilním vjemem při kondenzaci. Pro homogenní kondenzaci materiálu byla následně dokončena kondenzace materiálu sterilním papírovým čepem se zastřiženou špičkou (obr. 14). Je vhodné si takto upravený čep uchytit na původní pracovní délku, a při lehké kondenzaci tak můžeme vidět v jaké vzdálenosti od foramen apicale se nacházíme (obr. 15). Tyto dva kroky jsme opakovali, dokud jsme nedosáhli požadované tloušťky apikální zátky 5 mm. Následně jsme radiologicky ověřili homogenitu a umístění apikální zátky (obr. 16).
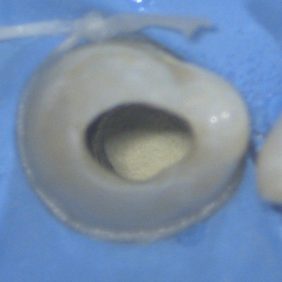
Po opakované kondenzaci papírovými čepy jsme zaplavili cavum pulpae a zbývající část kořenového kanálku fyziologickým roztokem a odstranili přebytky kalciumsilikátového cementu pomocí mikroštětečku. Následně jsme opakovaně zkondenzovali materiál pomocí zastřižených papírových čepů a cavum pulpae opískovali aluminiovým práškem (obr. 17). Je důležité odstranit veškeré zbytky kalciumsilikátového cementu z koronální části, abychom zamezili vzniku nežádoucích dyskolorací [5].
Po adhezivní přípravě zubu technikou total-etch a adhezivním systémem Optibond FL s dobou osvitu 60 sekund jsme vyzkoušeli pasivní dosed sklovláknových čepů DT Light Post (Bisco, Anaheim, USA) (obr. 18). Ty byly následně fixovány duálně tuhnoucím kompozitním materiálem BuildIt-FR (Pentron, Wallingford, USA) (obr. 19). Následně byly sklovláknové čepy i s dostavbovým materiálem zahloubeny cca 2 mm pod okraj přístupové kavity (obr. 20) a přelaminovány hydridním kompozitem Filtek Ultimate (3M ESPE, Maplewood, USA) (obr. 21).
Po ukončení výkonu byl zhotoven kontrolní intraorální rentgenový snímek, na kterém je viditelné oválné projasnění na rozhraní dostavby a kalciumsilikátového cementu (obr. 22). Jedná se o bublinu v duálně tuhnoucím kompozitním materiálu, která ale nebude mít klinicky významný dopad.
Při kontrolním vyšetření 6 měsíců po provedení výkonu byl pacient asymptomatický. Zub 22 byl poklepově nebolestivý stejně jako palpace v místě hrotu kořene zubu 22. Na kontrolním intraorálním rentgenovém snímku zubu 22 je viditelné hojení periapikálního nálezu kolem hrotu kořene zubu 22 (obr. 23). Pacient i nadále zůstává v dispenzární péči, dokud nedojde ke kompletnímu zhojení periapikálního nálezu.
Diskuze
Je nutné ihned na počátku diskuze vyzdvihnout, že neexistuje jediný správný postup, jak pracovat a manipulovat s kalciumsilikátovými cementy, a výsledek je velmi závislý na preciznosti, zkušenostech a důslednosti ošetřujícího lékaře (angl. operator sensitive). Výrobce udává jediné pokyny, a to pro poměr míchání tekutiny a prášku (1 : 3), ale vzhledem k velikosti dodávaných balení, která postačují na několik aplikací, dochází k situacím, kdy tekutina a prášek se smíchávají za neznámého poměru [6]. Výhodou ale je, že klinicky manipulovatelný materiál je připraven v rozmezí poměru prášku a tekutiny 1 : 3 až zhruba 1 : 4 (0,33–0,26). Pokud je materiál příliš suchý, nebo příliš tekutý, není možné jej prediktabilně dopravit do místa aplikace [7].
Při plnění kořenových kanálků pomocí pluggerů se doporučuje před samotným plněním vyzkoušet různé velikosti a vybrat takový, který se svojí velikostí co nejvíce blíží průměru foramen apicale a je možné jej volně, bez odporu zavést na pracovní délku zkrácenou o 0,5–1 mm [8, 9].
Pro lepší kondenzaci materiálu se v odborné literatuře velmi často zmiňuje použití ultrazvuku. Výsledky in vitro studií jsou poměrně rozdílné a občas i protichůdné. Část prací došla k závěru, že při použití ultrazvuku dochází k homogennějšímu rozložení částic [10-12], ale existují i práce, které zmiňují vyšší výskyt prázdných míst při kondenzaci pomocí ultrazvuku [13, 14], nebo které nenašly žádný rozdíl mezi technikami [15, 16]. Při dlouhodobějším použití ultrazvuku ale může docházet k zhoršení mechanických vlastností. Vysvětluje se to zahříváním, snižováním obsahu vody v materiálu a vyšším množstvím nezaplněných míst [13, 17]. Doba působení ultrazvuku při kondenzaci jednoho inkrementu by neměla přesáhnout 2 sekundy [17]. Doba tuhnutí, objemová expanze není změněna [10, 18].
Co se týče utěsnění, tak i v tomto případě existují studie, které nepozorovaly rozdíl [19], nebo udávají lepší utěsnění při použití ultrazvuku [20]. Při kondenzaci s pomocí ultrazvuku se udává vyšší vazba na tvrdé zubní tkáně [21], což je v souladu se zjištěním, že vazba je menší při využití materiálu s vyšším obsahem tekutiny při smíchání [22]. Je nutné ale zmínit, že záleží na použitém kalciumsilikátovém cementu, protože existují rozdíly mezi jednotlivými materiály při využití ultrazvuku při kondenzaci [23]. Z klinického hlediska musíme zdůraznit, že při neopatrném využití ultrazvuku může velmi snadno dojít k přetlačení kalciumsilikátového cementu do periapikální oblasti, což vzhledem k biokompatibilitě materiálu není možné brát jako komplikaci, ale na druhou stranu to rozhodně není žádoucí.
Kondenzace pomocí papírových čepů je v odborné literatuře poměrně málo zmiňovaná, i když se v klinické praxi používá poměrně často [9, 24, 25]. Výhodou tohoto postupu je odsátí přebytečné vody, čímž se materiál stává pevnější a lépe kondenzovatelný [26]. Na stejném principu se dají použít i mikroštětečky, které se ale hůře používají pro menší nasákavost a jejich větší rozměry. I přes poměrně časté klinické použití existuje pouze jediná in vitro studie, která se zabývala kvalitou utěsnění při kondenzaci papírovými čepy a nenašla signifikantní rozdíl oproti kondenzaci pluggery, nebo s pomocí ultrazvuku [19]. Z vlastní zkušenosti autorů a dostupných klinických referencí [27] nelze ale využít kondenzaci pomocí papírových čepů při využití materiálu Biodentin (Septodont, Saint-Maur-des-Fossés, Francie).
Největší z možných komplikací při využití kalciumsilikátových cementů je dyskolorace klinické korunky. Je nutné zmínit, že všechny kalciumsilikátové cementy mají určitou tendenci k dyskoloraci. Materiály s obsahem bizmutu mají tuto tendenci mnohonásobně větší [28]. Je to dáno reakcí bizmutu, který se uvolňuje z cementu [29] a dochází k jeho oxidaci při kontaktu s kolagenními vlákny [30]. Taktéž dochází k výraznější dyskoloraci při tuhnutí v kontaktu s chlornanem sodným nebo chlorhexidinem [5], a proto může být vhodné před zaplněním vypláchnout kořenový kanálek fyziologickým roztokem. Při ošetření, kdy aplikujeme kalciumsilikátový cement do koronální části kořenového kanálku (např. při hluboké pulpotomii nebo maturogenezi), je vhodné využít materiál neobsahující oxid bizmutitý. Vždy je ale nutné důkladně odstranit zbytky kalciumsilikátového cementu z povrchu cavum pulpae. Nejčastěji se očištění provádí pomocí mikroštětečků zvlhčených fyziologickým roztokem nebo vodou [27]. Po očištění stěn je vhodné opakovaně zkondenzovat materiál pomocí papírových čepů a následně povrch cavum pulpae opískovat. Povrch kalciumsilikátového cementu při kondenzaci a částečném vysušení papírovými čepy se stává mechanicky odolnější a nedochází ke ztrátě materiálu při opískování (nesmí ale dojít k nasměrování proudu přímo na kalciumsilikátový materiál).
V názoru na načasování zhotovení definitivní rekonstrukce a za jakých podmínek má být provedena, není ve světové literatuře všeobecná shoda. Část autorů se přiklání k odložení zhotovení definitivní rekonstrukce do doby, kdy bude materiál plně ztuhlý. Většinou až na druhý den, nebo později [31]. Někteří autoři preferují zhotovení definitivní rekonstrukce ihned a doporučují překrýt kalciumsilikátový cement buď gutaperčou, nebo skloionomerním cementem [24]. Při leptání kalciumsilikátových cementů pomocí kyseliny fosforečné dochází k negativnímu působení na porozitu materiálu, jeho tvrdost a odolnost v tlaku [32]. Je to dáno selektivní ztrátou matrix v okolí slinky, která ale nezasahuje do větší hloubky a nedochází k odplavení většího množství materiálu [33]. Také je důležité zmínit, že leptání nezlepšuje kvalitu vazby na kalciumsilikátové cementy [34], která je v podstatě zanedbatelná [35]. Z tohoto hlediska je nutné brát v potaz i možné komplikace vycházející z nedokonale zhotovené provizorní výplně, nebo horší spolupráce pacienta, kdy se nedostaví ke zhotovení definitivní rekonstrukce. V současné době nejsou žádné klinické studie, které by hodnotily vliv leptání a okamžité rekonstrukce na úspěšnost terapie [35]. Je nutné brát v potaz klinické zkušenosti a možnosti ošetřujícího lékaře a v případě pochybností nad kvalitou okamžitě zhotovené adhezivní rekonstrukce je vhodné se přiklonit spíše k dvoudobému postupu, nebo využít mezivrstvu z gutaperči nebo skloionomerního cementu.
Závěr
Při zpracování kalciumsilikátových cementů je potřeba postupovat jinak než u jiných materiálů, na které jsme v endodoncii a konzervačním zubním lékařství zvyklí. Je nutné striktně dodržovat pracovní postup k minimalizaci bublin a netěsností. Kondenzace s přímým nebo nepřímým působením ultrazvuku s největší pravděpodobností nevylepšuje klinický výsledek. Neméně důležité je i důkladné odstranění přebytků materiálu z cavum pulpae, neboť může dojít k esteticky nevyhovujícím dyskoloracím. Za určitých podmínek je možné a výhodné zub ihned adhezivně zrekonstruovat, i když ještě nedošlo ke ztuhnutí kalciumsilikátového cementu.
Obrazová dokumentace


Literatura
1. Lee SJ, Monsef M, Torabinejad M. Sealing ability of a mineral trioxide aggregate for repair of lateral root perforations. J Endod. 1993; 19(11): 541–544.
2. Žižka R, Šedý J, Škrdlant J, Kučera P. Kalciumsilikátové cementy. Část 2. Klinické využití. LKS. 2018; 28(3): 60–67.
3. Bogen G, Lawaty I, Chandler N. MTA root canal obturation. In: Torabinejad M, editor. Mineral Trioxide Aggregate: properties and clinical applications. 1.vydání. Oxford: Wiley Blackwell; 2014.
4. Oehlers FAC. Dens invaginatus (dilated composite odontome). I. Variations of the invagination process and associated anterior crown forms. Oral Surgery, Oral Med Oral Pathol. 1957; 10(11): 1204–1218.
5. Žižka R, Šedý J, Gregor L, Voborná I. Discoloration after regenerative endodontic procedures: A critical review. Iran Endod J. 2018; 13(3): 278-284.
6. Camilleri J. Composition and setting reaction. In: Camilleri J, editor. Mineral Trioxide Aggregate in dentistry. 1.vydání. Berlin: Springer; 2014.
7. Fridland M, Rosado R. Mineral Trioxide Aggregate (MTA) solubility and porosity with different water-to-powder ratios. J Endod. 2003; 29(12): 814–817.
8. Shabahang S, Witherspoon D. Management of teeth with necrotic pulp and open apices. In: Torabinejad M, editor. Mineral Trioxide Aggregate: properties and clinical applications. 1. vydání. Oxford: Wiley Blackwell; 2014.
9. Steinig TH, Regan JD, Gutmann JI. The use and predictable placement of Mineral Trioxide Aggregate® in one-visit apexification cases. Aust Endod J. 2003; 29(1): 34–42.
10. Duque J, Fernandes SL, Bubola J, Duarte M, Camilleri J, Marciano M. The effect of mixing method on tricalcium silicate-based cement. Int Endod J. 2018; 51(1): 69–78.
11. Yeung P, Liewehr FR, Moon PC. A quantitative comparison of the fill density of MTA produced by two placement techniques. J Endod. 2006; 32(5): 456–459.
12. Sisli SN, Ozbas H. Comparative micro–computed tomographic evaluation of the sealing quality of ProRoot MTA and MTA Angelus apical plugs placed with various techniques. J Endod. 2017; 43(1): 147–151.
13. Ghasemi N, Janani M, Razi T, Atharmoghaddam F. Effect of different mixing and placement methods on the quality of MTA apical plug in simulated apexification model. J Clin Exp Dent. 2017; 9(3): 351–355.
14. Aminoshariae A, Hartwell GR, Moon PC. Placement of mineral trioxide aggregate using two different techniques. J Endod. 2003; 29(10): 679–682.
15. Keleş A, Torabinejad M, Keskin C, Sah D, Uzun İ, Alçin H. Micro-CT evaluation of voids using two root filling techniques in the placement of MTA in mesial root canals of Vertucci type II configuration. Clin Oral Investig. 2018; 22(5): 1907–1913.
16. Küçükkaya Eren S, Aksel H, Askerbeyli Örs S, Serper A, Koçak Y, Ocak M, et al. Obturation quality of calcium silicate-based cements placed with different techniques in teeth with perforating internal root resorption: a micro-computed tomographic study. Clin Oral Investig. 2018; Epub ahead.
17. Parashos P, Phoon A, Sathorn C. Effect of Ultrasonication on physical properties of Mineral Trioxide Aggregate. Biomed Res Int. 2014; ID 191984.
18. Shahi S, Ghasemi N, Rahimi S, Yavari H, Janani M, Mokhtari H, et al. The effect of different mixing methods on working time, setting time, dimensional changes and film thickness of Mineral Trioxide Aggregate and calcium-enriched mixture. Iran Endod J. 2015; 10(4): 248–251.
19. Alhaddad Alhamoui F, Steffen H, Splieth CH. The sealing ability of ProRoot MTA when placed as an apical barrier using three different techniques: an in-vitro apexification model. Quintessence Int. 2014; 45(10): 821–827.
20. Kim US, Shin SJ, Chang SW, Yoo HM, Oh TS, Park DS. In vitro evaluation of bacterial leakage resistance of an ultrasonically placed Mineral Trioxide Aggregate orthograde apical plug in teeth with wide open apexes: a preliminary study. Oral Surgery, Oral Med Oral Pathol Oral Radiol Endodontology. 2009; 107(4): 52–56.
21. Küçükkaya Eren S, Aksel H, Serper A. Effect of placement technique on the push-out bond strength of calcium-silicate based cements. Dent Mater J. 2016; 35(5): 742–747.
22. Türker SA, Uzunoğlu E. Effect of powder-to-water ratio on the push-out bond strength of white Mineral Trioxide Aggregate. Dent Traumatol. 2016; 32(2): 153–155.
23. Basturk FB, Nekoofar MH, Gunday M, Dummer PMH. X-ray diffraction analysis of MTA mixed and placed with various techniques. Clin Oral Investig. 2018; 22(4): 1675–1680.
24. Bogen G, Kuttler S. Mineral Trioxide Aggregate obturation: a review and case series. J Endod. 2009; 35(6): 777–790.
25. Raldi DP, Mello I, Habitante SM, Luiz Lage-Marques J, Coil J. Treatment options for teeth with open apices and apical periodontitis. J Can Dent Assoc. 2009; 75(8): 591–596.
26. Roda R, Gettleman B. Nonsurgical retreatment. In: Hargreaves KM, editor. Cohen’s pathway to pulp. 11. vydání. St. Louis: Elsevier; 2015.
27. Ree MH. Clinical management of teeth with open apices with the apical barrier technique. In: Schwartz RS, Canakapalli V, editors. Best practise in endodontics: a desk reference. 1.vydání. Hanover Park: Quintessence; 2015.
28. Możyńska J, Metlerski M, Lipski M, Nowicka A. Tooth discoloration induced by different calcium silicate–based cements: a systematic review of in vitro studies. J Endod. 2017; 43(10): 1593–1601.
29. Camilleri J. Characterization of hydration products of Mineral Trioxide Aggregate. Int Endod J. 2008; 41(5): 408–17.
30. Marciano MA, Duarte MAH, Camilleri J. Dental discoloration caused by bismuth oxide in MTA in the presence of sodium hypochlorite. Clin Oral Investig. 2015; 19(9): 2201–2209.
31. Ree MH, Schwartz RS. Long-term success of nonvital, immature permanent incisors treated with a Mineral Trioxide Aggregate plug and adhesive restorations: a case series from a private endodontic practice. J Endod. 2017; 43(8): 1370–1377.
32. Camilleri J, Dummer PM. Reactivity and environmental factors. In: Camilleri J, editor. 1. vydání. Berlin: Springer; 2014.
33. Kayahan MB, Nekoofar MH, Kazandağ M, Canpolat C, Malkondu O, Kaptan F, et al. Effect of acid-etching procedure on selected physical properties of Mineral Trioxide Aggregate. Int Endod J. 2009; 42(11): 1004–1014.
34. Oskoee SS, Kimyai S, Bahari M, Eghbal PMMJ, Asgary S. Comparison of shear bond strength of calcium-enriched mixture cement and Mineral Trioxide Aggregate to composite resin. J Contemp Dent Pract. 2011; 12(6): 457–462.
35. Meraji N, Camilleri J. Bonding over dentin replacement materials. J Endod. 2017; 43(8):
15. 2. 2020
Print: LKS. 2020; 30(2): 26 – 31
Autoři:
Fotografie
- Radovan Žižka
Rubrika:
Téma: