Kalciumsilikátové cementy – 1. část: Vlastnosti a rozdělení
Přehledové sdělení
Souhrn: Kalciumsilikátové cementy tvoří nezbytnou součást vybavení každého praktického zubního lékaře, který se hlouběji zajímá o endodoncii a konzervační zubní lékařství. Od roku 1997, kdy byl uveden na trh první materiál této skupiny – ProRoot MTA (Dentsply, Tulsa, USA), se objevilo velké množství materiálů patřících do této skupiny. Cílem první části tohoto sdělení je shrnout chemické, fyzikální a biologické vlastnosti kalciumsilikátových cementů, které stojí za jejich vynikajícími klinickými vlastnostmi. Tato část sdělení se rovněž zabývá rozdělením kalciumsilikátových cementů.
Klíčová slova: MTA, Biodentin, Totalfill, kalciumsilikátové cementy
Calcium silicate cements – Part 1: properties and classification
Review article
Summary: Calcium silicate cements represent an integral piece of equipment of every general dentist who is more deeply interested in endodontics and restorative dentistry. Since 1997, when the first calcium silicate cement – ProRoot MTA (Dentsply, Tulsa, USA) – was introduced to market many materials belonging to the calcium silicate cement group have appeared. The aim of the first part of the review is to summarize the chemical, physical, and biologi cal pr operties of calcium silicate cements that are responsible for their outstanding clinical characteristics. Furthermore, this section also deals with the division of calcium silicate cements into particular groups.
Key words: MTA, Biodentin, Totalfill, calcium silicate cements
Úvod
V endodoncii se vždy vyskytovaly klinické situace, které měly i při vysoké zručnosti a zkušenosti ošetřujícího lékaře velmi nejasnou prognózu (např. krytí perforací). Za selhání byly v těchto případech odpovědné bakterie a jejich toxiny, které pronikaly skrz či kolem netěsnící kořenové výplně do periodoncia. Jednou z hlavních příčin, proč vznikaly tyto netěsnosti, byla přítomnost vlhkého prostředí při tuhnutí kořenové výplně, a tedy i nedokonalé ztuhnutí materiálu a špatná marginální adaptace. Od roku 1993, kdy byl poprvé popsán materiál MTA (angl. mineral trioxide aggregate) jako materiál vhodný na překrytí perforací vzniklých při endodontickém ošetření (1), se rozšířilo indikační spektrum využití kalciumsilikátových cementů na retrográdní plnění při chirurgické endodoncii, přímé překrytí zubní dřeně, pulpotomii, plnění kořenových kanálků u zubů s neukončeným vývojem, léčbu dentálních anomálií nebo zaplnění kavit vzniklých vnější resorpcí (2). S postupem času se ale také na trhu objevilo nepřeberné množství materiálů, které se s materiálem MTA porovnávají či se na něj odvolávají (a někdy neprávem).
Základem materiálu MTA a potažmo i kalciumsilikátových cementů je portlandský cement, což bylo zmíněno i v původním patentu, kde obsahoval zhruba 75 % hmotnosti materiálu MTA. Je nutné podotknout, že dle amerických norem existuje celkem 10 typů portlandského cementu, přičemž portlandský cement využitý v MTA je pouze prvním typem (ASTM Standart C150/C150M – 12 2012 dle Americké společnosti pro testování a materiály). Historie využití portlandského cementu sahá ale mnohem hlouběji do historie. Poprvé se zmiňuje jeho využití pro plnění kořenových kanálků a přímé překrytí zubní dřeně již v 70. letech 19. století (3, 4), ale i přes údajnou vysokou úspěšnost se cement nedočkal širšího uplatnění, a tak si na uvedení na trh musel počkat až do roku 1997. Autoři zdůrazňují, že i když je portlandský cement základem kalciumsilikátových cementů, vlastnosti nemedicinálního portlandského cementu jsou velmi rozdílné v závislosti na využitém typu a způsobu přípravy. Mimo jiné i proto je využívání nemedicínského portlandského cementu v medicíně zcela nepřípustné.
Chemické vlastnosti
Složení
Jako hlavní složka původního materiálu MTA se udává portlandský cement, který zaujímá zhruba 75 % hmotnosti MTA. Dále je přítomen oxid bizmutitý (20 %), přidávaný pro zvýšení radiopacity, a sádra (5 %), která účinkuje jako regulátor tuhnutí. U nových generací kalciumsilikátových cementů došlo nahrazením některých sloučenin či jiných příměsí ke zlepšení mechanických vlastností a omezení dyskolorací (tab. I).
Tabulka I: Porovnání kalciumsilikátových cementů – pH a složení
| Sloučenina | MTA | Bioaggregate | Biodentin | Totalfill |
| trikalciumsilikát | + | + | + | + |
| dikalciumsilikát | + | + | + | + |
| trikalciumaluminát | + | - | - | - |
| oxid bizmutitý | + | - | - | - |
| oxid zirkoničitý | - | - | + | + |
| oxid tantaličný | - | + | - | + |
| sádra | + | - | - | - |
| uhličitan vápenatý | - | - | + | - |
| hydrogen fosforečnan vápenatý | - | - | - | + |
| chlorid vápenatý | - | - | + | - |
Výjimečná vlastnost kalciumsilikátových cementů v rámci zubního lékařství spočívá v tom, že patří mezi tzv. hydraulická pojiva. To znamená, že reagují s vodou a následně v nich po proběhlé reakci zachovávají svoji pevnost a stálost.
- Trikalciumsilikát (alit)/dikalciumsilikát (belit). Jedná se o hlavní složky, které dávají i jméno této skupině cementů. Tyto dvě sloučeniny tvoří zhruba 75–80 % původního portlandského cementu. Reakce dikalciumsilikátu je oproti trikalciumsilikátu pomalejší. To stejné platí i o růstu pevnosti.
- Trikalciumaluminát. Vyznačuje se zvýšenou reaktivitou s vodou, rychlým tuhnutím a tvrdnutím (5). Jeho obsah je ale oproti výše zmíněným složkám výrazně nižší a pohybuje se pod 10 % objemu cementu (6). Na rozdíl od původního materiálu ProRoot je v moderních generacích jeho množství zanedbatelné (7).
- Tetrakalciumaluminoferit (celit). Jeho procentuální zastoupení v původním portlandském cementu je podobné jako u trikalciumaluminátu a pohybuje se pod 10 % (6). Tato sloučenina se vyznačuje pomalejším růstem pevnosti (5).
- Oxid bizmutitý. V původním materiálu ProRoot MTA zaujímal téměř 20 % (8). Jeho hlavním účelem je dostatečná rentgenkontrastnost materiálu, jelikož výše zmíněné silikáty rentgenkontrastní nejsou. I když se původně předpokládalo, že je nerozpustný ve vodě a nebude ovlivňovat probíhající reakci, prokázalo se, že může nahradit křemík ve struktuře kalciumsilikáthydrátu (9), a že ovlivňuje precipitaci hydroxidu vápenatého po hydrataci materiálu MTA (10). Oxid bizmutitý se ale rozpouští v kyselém prostředí a může se při aplikaci materiálu MTA do blízkosti zánětlivé tkáně uvolnit (10), což může snížit biokompatibilitu takovéhoto kalciumsilikátového cementu. U moderních materiálů slouží jako rentgenkontrastní plnivo oxid zirkoničitý (Biodentin, Totalfill), nebo oxid tantaličný (Totalfill).
- Sádra. Zatím nebylo prokázáno, ve které formě je sádra přítomna, neboť i literatura je v tomto směru poměrně nejasná (8, 10, 11). V původním materiálu ProRoot je přítomna zhruba v 5 % hmotnosti a její množství je tím oproti původnímu portlandskému cementu zhruba poloviční. Prodlužuje dobu tuhnutí, a to tím, že ovlivňuje chemickou reakci trikalcium aluminátu s vodou (12).
- Uhličitan vápenatý. Jde o významnou příměs u Biodentinu (Septodont, Francie). Částice uhličitanu vápenatého jsou poměrně velké oproti ostatním částicím prášku a hydratační produkty jsou přítomny okolo krystalů uhličitanu vápenatého. Tím mění jeho mikrostrukturu, neboť funguje jako nukleační místo (13, 14). Také urychluje tuhnutí, ale snižuje sílu v kompresi a udává se vyšší rozpustnost materiálu (15).
- Oxid zirkoničitý. Sloučenina, která je u Biodentinu (Septodont, Francie) zodpovědná za rentgenkontrastnost a mechanické vlastnosti, jež jsou řádově vyšší než u ostatních kalciumsilikátových cementů. Na rozdíl od oxidu bizmutitého se považuje za biokompatibilní sloučeninu odolnou vůči korozi (16). V menším množství je obsažen u materiálů třetí generace kalciumsilikátových cementů, kde ale není hlavní sloučeninou zodpovědnou za rentgenkontrastnost.
- Oxid tantaličný. Je zodpovědný za rentgenkontrastnost u materiálů třetí generace kalciumsilikátových cementů.
- Hydrogenfosforečnan vápenatý. Je to významná složka u nejmodernější generace kalciumsilikátových cementů, nicméně je přítomný i u BioAggregate (Brassler, USA), který jim časově předcházel. V prvním týdnu umocňuje vznik apatitových precipitátů na povrchu materiálu (17) díky svému obsahu fosforečnanové skupiny, která u původního materiálu není přítomna (18–20). To se může projevit lepší vazbou na dentin.
Tuhnutí
U všech současných materiálů probíhá hlavní reakce, kdy reaguje trikalciumsilikát s vodou a vzniká hydratovaný kalciumsilikát v gelové fázi (angl. calcium silicate hydrat, C-S-H) s hydroxidem vápenatým:
3CaO ∙ SiO2 + H20 → C-S-H + Ca(OH)2
Pokud je přítomen i dikalciumsilikát, probíhá reakce velmi podobně:
2CaO ∙ SiO2 + 4H20 → C-S-H + Ca(OH)2
Prostředí, které takto vzniká, je zásadité a liší se mezi jednotlivými materiály zanedbatelně (tab. II). Kde ale existuje výrazný rozdíl, je doba tuhnutí, kdy u Biodentinu díky příměsi katalyzátoru chloridu vápenatého dochází k výraznému urychlení reakce (tab. II).
Tabulka II: Porovnání kalciumsilikátových cementů – fyzikální vlastnosti
| Vlastnosti | MTA | Bioaggregate | Biodentin | Totalfill |
| Velikost částic | velká | malá | malá | malá |
| Čas tuhnutí | 3 hod. | 4 hod. | 12 min. | 3-4 hod. |
| Náročnost na manipulaci | vysoká | vysoká | střední | nízká |
| Pevnost v tlaku | 45-98 MPa | 60-70 MPa | 300-350 MPa | 50-70 Mpa |
| Rentgenkontrastnost |
4,5-7,1 mm Al |
2,7-3,78 mmAl |
3,08-3,92 mm Al |
3,84 mm Al |
|
Dyskolorace |
ano |
ne |
ne |
ne |
|
pH |
12,8 |
12,8 |
12,9 |
12,7 |
Nicméně ne všechny částice kalciumsilikátového cementu plně zreagují a nezreagovaný prášek může být přítomný i za sedm (21) nebo 30 dní (9). Taktéž dochází postupem času ke zrání neboli maturaci kalciumsilikátových cementů. Bylo prokázáno, že kalciumsilikátový cement má po delším časovém úseku lepší mechanické vlastnosti než po jednom dni (22–24).
Reakce s dentinem, tvorba apatitové struktury a specifické mezivrstvy
(angl. interfacial layer)
Od počátku využívání kalciumsilikátových cementů byla zmiňována vynikající schopnost utěsnění oproti ostatním materiálům v podobných indikacích. Až později se zjistilo, že pokud je kalciumsilikátový cement uchováván ve fosfátovém pufru, vytváří se na něm precipitáty (19). Při podrobnějším zkoumání se zjistilo, že chemicky se jedná o apatitové struktury velmi podobné hydroxyapatitu (25–27). Navíc byla zjištěna výše zmíněná specifická mezivrstva, která se tvoří mezi kalciumsilikátovým cementem a dentinem (25) (obr. 1). Tato vrstva je důsledkem chemické reakce vápenatých kationtů z hydroxidu vápenatého, který vzniká při reakci trikalciumsilikátu s vodou, a fosforečnatých aniontů. Bylo prokázáno, že těsnost kalciumsilikátových cementů a potažmo jejich vazba na dentin je vyšší, pokud tuhnou za přítomnosti fosfátového pufru než při kontaktu s destilovanou vodou (28). Taktéž přítomnost hydrogenfosforečnanu vápenatého urychluje tvorbu precipitátů, neboť z něho vzniká apatit (29).
Fyzikální vlastnosti
Rozpustnost
Žádanou vlastností kořenové výplně je, aby nebyla rozpustná a naopak byla prostorově stabilní. I když existují drobné rozpory mezi studiemi, většina ukazuje minimální nebo téměř žádnou rozpustnost materiálu MTA (22, 30–33). Nicméně existují i důkazy, že materiál MTA dlouhodobě exponovaný vlhkým prostředím může být náchylnější k rozpuštění (34), což potvrzuje ojedinělé případy resorpce extrudovaného materiálu.
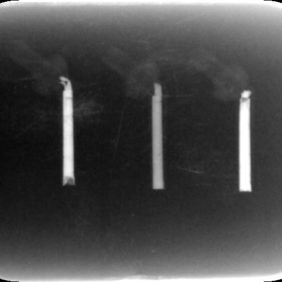
Radioopacita
Mezi různými materiály existují velké rozdíly v radioopacitě, které se odvíjejí od využitého rentgenkontrastního materiálu. Mezi materiály jsou poměrně velké rozdíly (obr. 2). Velmi dobře rentgenkontrastní materiály jsou 1. a 3. generace. Poměrně málo rentgenkontrastním materiálem je Biodentin. I když podstatná část studií udává, že má vyhovující rentgenkontrastnost odpovídající větší tloušťce, než jsou 3 mm hliníkové fólie, což je bráno jako minimální rentgenkontrastnost materiálu kořenové výplně (13), tak při klinickém použití je velmi obtížné rozeznat materiál Biodentin od dentinu (14). Toto zjištění bylo následně potvrzeno novějšími studiemi (35, 36).
Expanze při tuhnutí
Kromě výše zmíněného vzniku mezivrstvy mezi kalciumsilikátovým cementem a dentinem se na velmi dobré těsnosti podílí i expanze materiálu při tuhnutí. Zdá se, že původní šedá varianta ProRoot MTA má vyšší jak lineární (37), tak volumetrickou (38) expanzi při tuhnutí, i když to nebylo potvrzeno jinými studiemi (30, 39). Toto zjištění je v současné době zbytečné, jelikož je na trhu pouze bílá varianta ProRoot MTA. Nicméně k expanzi dochází např. i u Biodentinu (40), a lze tak předpokládat, že u ostatních kalciumsilikátových cementů tomu nebude jinak.
Tvrdost
(se zaměřením na korelaci s kvalitou tuhnutí)
Tvrdost materiálu je vlastnost vztažená k odporu proti pronikání cizího tělesa a u kalciumsilikátových cementů může být ovlivněna různými faktory. Mezi tyto faktory patří vlastnosti okolního prostředí jako pH (41, 42), teplota (21), vlhkost (43) nebo tloušťka materiálu (44), kvalita kondenzace (45), přítomnost chelatačního prostředku a leptání povrchu materiálu kyselinou fosforečnou (46, 47). Podstatné je, že je tvrdost materiálu brána jako udavatel kvality hydratačních procesů a proběhlého tuhnutí kalciumsilikátových cementů (21, 42). Současné poznatky naznačují, že při méně vlhkém prostředí, nižších hodnotách pH, přítomnosti chelatačního činidla nebo velmi homogenní kondenzaci materiálu hydratační procesy neprobíhají optimálně a následná tvrdost ztuhlého kalciumsilikátového cementu je nižší. Tento fakt se může následně projevit horší těsností materiálu.
Optické vlastnosti
Jednou z hlavních nevýhod některých starších kalciumsilikátových cementů (zvláště materiálů MTA) je jejich potenciál k dyskoloracím zubů. Poprvé byly tyto estetické komplikace popsány v souvislosti s pulpotomiemi dočasných molárů (48, 49), neboť při aplikaci hluboko do kořenového systému nebo při retrográdní chirurgii se tyto dyskolorace klinicky neprojevily, i když byly laboratorně potvrzeny (50). Zvláště s nástupem maturogeneze byly popisovány nežádoucí dyskolorace stále častěji (51). Zpočátku byly jako možné příčinné faktory dyskolorací zmiňovány soli železa a manganu (7, 52). I po úpravě složení, kdy byly tyto prvky téměř eliminovány (např. materiál ProRoot MTA white), však zůstává tendence k dyskoloracím téměř stejná (53). Tyto dyskolorace jsou výraznější, pokud je materiál v kontaktu s chlornanem sodným (54) nebo krví (55). Nejpravděpodobnějším zdrojem těchto dyskolorací se zdá být oxid bismutitý (54). Ostatní materiály z této skupiny, které neobsahují oxid bismutitý, tendenci k dyskoloracím nemají (56).
Biologické vlastnosti
Antibakteriální vlastnosti
I přes větší množství protichůdných studií lze vyvodit závěr, že MTA má antimikrobiální a antimykotické působení. Tyto protichůdné výsledky jsou z velké části důsledkem použití různých druhů mikroorganismů a přípravy materiálu MTA v jednotlivých studiích (57). Pravděpodobným mechanismem tohoto antimikrobiálního působení je vznik Ca(OH)2 a zvýšené pH při tuhnutí materiálu (58–60).
Biokompatibilita
Bezpočet in vitro studií prokázalo, že kalciumsilikátové cementy jsou biokompatibilními materiály. Studiemi na buněčných kulturách se sleduje cytotoxické působení materiálu vzhledem k životaschopnosti buněk, aktivita alkalické fosfatázy nebo množství odloučených buněk. Velmi dobře biokompatibilním materiálem je MTA (61–63) a podobně se chovají i materiály novějších generací jako Biodentin (64) nebo zástupci 3. generace, a to jak ve formě sealeru (65), tak materiálu na opravu perforací (66).
Působení na kmenové buňky zubní dřeně
V rámci výkonů se zachováním vitality zubní dřeně může dojít k jejímu odhalení a poškození. Za určitých podmínek mohou nediferencované mezenchymální kmenové buňky opustit svoji perivaskulární niku a následně diferencovat v buňky podobné odontoblastům, které mohou produkovat osteodentin. Kromě výborného utěsnění díky expanzi při tuhnutí a vzniku apatitové mezivrstvy disponují ještě schopností částečně ovlivnit diferenciaci kmenových buněk v buňky podobné odontoblastům a schopností jejich mineralizace (67, 68) a zároveň se zvyšuje i míra proliferace nediferencovaných buněk a buněk podobných odontoblastům (69).
Obrazová dokumentace
Literatura
1. Lee SJ, Monsef M, Torabinejad M. Sealing ability of a mineral trioxide aggregate for repair of lateral root perforations. J Endod, 1993, 19(11): 541–544.
2. Haapasalo M, Parhar M, Huang X, Wei X, Lin J, Shen Y. Clinical use of bioceramic materials. Endod Topics, 2015, 32(1): 97–117.
3. Witte D. Das füelen der wurzelkanäle mit Portland-cement. Deutsche Vierteljahrschrifft fuer Zahnheilkunde, 1878, 18(3): 153–154.
4. Schlenker D. Das füelen der wurzelkanäle mit Portland- cement nach Dr. Witte. Deutsche Vierteljahrschrifft fuer Zahnheilkunde, 1880, 20(4): 277–283.
5. Škvára F. Technologie anorganických pojiv I, část 1. Vysoká škola chemicko-technologická, Praha, 1994, 303.
6. Ramachandran VS, Paroli RM, Beaudoin JJ. Handbook of Thermal Analysis of Construction Materials. Noyes Publication/ William Andrew Publishing, New York, 2003.
7. Asgary S, Parirokh M, Eghbal MJ, Brink F. Chemical differences between white and gray mineral trioxide aggregate. J Endod, 2005, 31(2): 101–103.
8. Reyes-Carmona JF, Felippe MS, Felippe WT. Biomineralization ability and interaction of mineral trioxide aggregate and white portland cement with dentin in a phosphate-containing fluid. J Endod, 2009, 35(5): 731–736.
9. Camilleri J. Characterization of hydration products of mineral trioxide aggregate. Int Endod J, 2008, 41(5): 408–417.
10. Camilleri J. Hydration mechanisms of mineral trioxide aggregate. Int Endod J, 2007, 40(6): 462–470.
11. Gandolfi MG, Taddei P, Tinti A, Prati C. Apatite-forming ability (bioactivity) of ProRoot MTA. Int Endod J, 2010, 43(10): 917–929.
12. Berzins DW. Chemical Properties of MTA. In: Torabinejad M, editor. Mineral trioxide aggregate: properties and clinical applications. John Wiley & Sons, 2014, 17–36.
13. Grech L, Mallia B, Camilleri J. Characterization of set intermediate restorative material, biodentine, bioaggregate and a prototype calcium silicate cement for use as root-end filling materials. Int Endod J, 2013, 46(7): 632–641.
14. Malkondu O, Karapinar Kazandag M, Kazazoglu E. A review on biodentine, a contemporary dentine replacement and repair material. Biomed Res Int, 2014, 2014: 160951.
15. Bernardi A, Bortoluzzi EA, Felippe WT, Felippe MC, Wan WS, Teixeira CS. Effects of the addition of nanoparticulate calcium carbonate on setting time, dimensional change, compressive strength, solubility and pH of MTA. Int Endod J, 2015 [Epub ahead print].
16. Piconi C, Maccauro G. Zirconia as a ceramic biomaterial. Biomaterials, 1999, 20(1): 1–25.
17. Shokouhinejad N, Nekoofar MH, Razmi H, Sajadi S, Davies TE, Saghiri MA, et al. Bioactivity of EndoSequence root repair material and bioaggregate. Int Endod J, 2012, 45(12): 1127–1134.
18. Asgary S, Parirokh M, Eghbal MJ, Brink F. A comparative study of white mineral trioxide aggregate and white Portland cements using X-ray microanalysis. Aust Endod J, 2004, 30(3): 89–92.
19. Camilleri J, Montesin FE, Brady K, Sweeney R, Curtis RV, Ford TR. The constitution of mineral trioxide aggregate. Dent Mater, 2005, 21(4): 297–303.
20. Camilleri J, Pitt Ford TR. Mineral trioxide aggregate: a review of the constituents and biological properties of the material. Int Endod J, 2006, 39(10): 747–754.
21. Lee YL, Lee BS, Lin FH, Yun Lin A, Lan WH, Lin CP. Effects of physiological environments on the hydration behavior of mineral trioxide aggregate. Biomaterials, 2004, 25(5): 787–793.
22. Torabinejad M, Hong CU, McDonald F, Pitt Ford TR. Physical and chemical properties of a new root-end filling material. J Endod, 1995, 21(7): 349–353.
23. Sluyk SR, Moon PC, Hartwell GR. Evaluation of setting properties and retention characteristics of mineral trioxide aggregate when used as a furcation perforation repair material. J Endod, 1998, 24(11): 768–771.
24. Vanderweele RA, Schwartz SA, Beeson TJ. Effect of blood contamination on retention characteristics of MTA when mixed with different liquids. J Endod, 2006, 32(5): 421–424.
25. Sarkar NK, Caicedo R, Ritwik P, Moiseyeva R, Kawashima I. Physicochemical basis of the biologic properties of mineral trioxide aggregate. J Endod, 2005, 31(2): 97–100.
26. Bozeman TB, Lemon RR, Eleazer PD. Elemental analysis of crystal precipitate from gray and white MTA. J Endod, 2006, 32(5): 425–428.
27. Reyes-Carmona JF, Felippe MS, Felippe WT. The biomineralization ability of mineral trioxide aggregate and Portland cement on dentin enhances the push-out strength. J Endod, 2010, 36(2): 286–291.
28. Reyes-Carmona JF, Felippe MS, Felippe WT. A phosphate-buffered saline intracanal dressing improves the biomineralization ability of mineral trioxide aggregate apical plugs. J Endod, 2010, 36(10): 1648–1652.
29. Tay FR, Pashley DH, Rueggeberg FA, Loushine RJ, Weller RN. Calcium phosphate phase transformation produced by the interaction of the portland cement component of white mineral trioxide aggregate with a phosphate-containing fluid. J Endod, 2007, 33(11): 1347–1351.
30. Islam I, Chng HK, Yap AU. Comparison of the physical and mechanical properties of MTA and portland cement. J Endod, 2006, 32(3): 193–197.
31. Poggio C, Lombardini M, Alessandro C, Simonetta R. Solubility of root-end-filling materials: a comparative study. J Endod, 2007, 33(9): 1094–1097.
32. Shie MY, Huang TH, Kao CT, Huang CH, Ding SJ. The effect of a physiologic solution pH on properties of white mineral trioxide aggregate. J Endod, 2009, 35(1): 98–101.
33. Danesh G, Dammaschke T, Gerth HU, Zandbiglari T, Schafer E. A comparative study of selected properties of ProRoot mineral trioxide aggregate and two Portland cements. Int Endod J, 2006, 39(3): 213–219.
34. Fridland M, Rosado R. MTA solubility: a long term study. J Endod, 2005, 31(5): 376–379.
35. Tanalp J, Karapinar-Kazandag M, Dolekoglu S, Kayahan MB. Comparison of the radiopacities of different root-end filling and repair materials. Sci World J, 2013, 2013: 594950.
36. Kaup M, Schafer E, Dammaschke T. An in vitro study of different material properties of Biodentine compared to ProRoot MTA. Head Face Med, 2015, 11: 16.
37. Storm B, Eichmiller FC, Tordik PA, Goodell GG. Setting expansion of gray and white mineral trioxide aggregate and Portland cement. J Endod, 2008, 34(1): 80–82.
38. Hawley M, Webb TD, Goodell GG. Effect of varying water- to-powder ratios on the setting expansion of white and gray mineral trioxide aggregate. J Endod, 2010, 36(8): 1377–1379.
39. Chng HK, Islam I, Yap AU, Tong YW, Koh ET. Properties of a new root-end filling material. J Endod, 2005, 31(9): 665–668.
40. Koubi S, Elmerini H, Koubi G, Tassery H, Camps J. Quantitative evaluation by glucose diffusion of microleakage in aged calcium silicate-based open-sandwich restorations. Int J Dent, 2012, 2012: 105863.
41. Namazikhah MS, Nekoofar MH, Sheykhrezae MS, Salariyeh S, Hayes SJ, Bryant ST, et al. The effect of pH on surface hardness and microstructure of mineral trioxide aggregate. Int Endod J, 2008, 41(2): 108–116.
42. Bolhari B, Nekoofar MH, Sharifian M, Ghabrai S, Meraji N, Dummer PM. Acid and microhardness of mineral trioxide aggregate and mineral trioxide aggregate-like materials. J Endod, 2014, 40(3): 432–435.
43. Caronna V, Himel V, Yu Q, Zhang JF, Sabey K. Comparison of the surface hardness among 3 materials used in an experimental apexification model under moist and dry environments. J Endod, 2014, 40(7): 986–989.
44. Matt GD, Thorpe JR, Strother JM, McClanahan SB. Comparative study of white and gray mineral trioxide aggregate (MTA) simulating a one- or two-step apical barrier technique. J Endod, 2004, 30(12): 876–879.
45. Nekoofar MH, Adusei G, Sheykhrezae MS, Hayes SJ, Bryant ST, Dummer PM. The effect of condensation pressure on selected physical properties of mineral trioxide aggregate. Int Endod J, 2007, 40(6): 453–461.
46. Kayahan MB, Nekoofar MH, Kazandag M, Canpolat C, Malkondu O, Kaptan F, et al. Effect of acid-etching procedure on selected physical properties of mineral trioxide aggregate. Int Endod J, 2009, 42(11): 1004–1014.
47. Lee YL, Lin FH, Wang WH, Ritchie HH, Lan WH, Lin CP. Effects of EDTA on the hydration mechanism of mineral trioxide aggregate. J Dent Res, 2007, 86(6): 534–538.
48. Naik S, Hegde AH. Mineral trioxide aggregate as a pulpotomy agent in primary molars: an in vivo study. J Indian Soc Pedod Prev Dent, 2005, 23(1): 13–16.
49. Maroto M, Barberia E, Planells P, Garcia Godoy F. Dentin bridge formation after mineral trioxide aggregate (MTA) pulpotomies in primary teeth. Am J Dent, 2005, 18(3): 151–154.
50. Boutsioukis C, Noula G, Lambrianidis T. Ex vivo study of the efficiency of two techniques for the removal of mineral trioxide aggregate used as a root canal filling material. J Endod, 2008, 34(10): 1239–1242.
51. Nosrat A, Homayounfar N, Oloomi K. Drawbacks and unfavorable outcomes of regenerative endodontic treatments of necrotic immature teeth: a literature review and report of a case. J Endod, 2012, 38(10): 1428–1434.
52. Dammaschke T, Gerth HU, Zuchner H, Schafer E. Chemical and physical surface and bulk material characterization of white ProRoot MTA and two Portland cements. Dent Mater, 2005, 21(8): 731–738.
53. Watts JD, Holt DM, Beeson TJ, Kirkpatrick TC, Rutledge RE. Effects of pH and mixing agents on the temporal setting of tooth-colored and gray mineral trioxide aggregate. J Endod, 2007, 33(8): 970–973.
54. Marciano MA, Duarte MA, Camilleri J. Dental discoloration caused by bismuth oxide in MTA in the presence of sodium hypochlorite. Clin Oral Investig, 2015, 19(9): 2201–2209.
55. Felman D, Parashos P. Coronal tooth discoloration and white mineral trioxide aggregate. J Endod, 2013, 39(4): 484–487.
56. Kohli MR, Yamaguchi M, Setzer FC, Karabucak B. Spectrophotometric analysis of coronal tooth discoloration induced by various bioceramic cements and other endodontic materials. J Endod, 2015, 41(11): 1862–1866.
57. Parirokh M, Torabinejad M. Mineral trioxide aggregate: a comprehensive literature review –Part I: chemical, physical, and antibacterial properties. J Endod, 2010, 36(1): 16–27.
58. Parirokh M, Torabinejad M. Mineral trioxide aggregate: a comprehensive literature review – Part III: Clinical applications, drawbacks, and mechanism of action. J Endod, 2010, 36(3): 400–413.
59. Eldeniz AU, Hadimli HH, Ataoglu H, Orstavik D. Antibacterial effect of selected root-end filling materials. J Endod, 2006, 32(4): 345–349.
60. Tanomaru-Filho M, Tanomaru JM, Barros DB, Watanabe E, Ito IY. In vitro antimicrobial activity of endodontic sealers, MTA-based cements and Portland cement. J Oral Sci, 2007, 49(1): 41–45.
61. Gorduysus M, Avcu N, Gorduysus O, Pekel A, Baran Y, Avcu F, et al. Cytotoxic effects of four different endodontic materials in human periodontal ligament fibroblasts. J Endod, 2007, 33(12): 1450–1454.
62. Huang TH, Yang CC, Ding SJ, Yan M, Chou MY, Kao CT. Biocompatibility of human osteosarcoma cells to root end filling materials. Part B, Applied biomaterials. J Biomed Mater Res, 2005, 72(1): 140–145.
63. Zhu Q, Haglund R, Safavi KE, Spangberg LS. Adhesion of human osteoblasts on root-end filling materials. J Endod, 2000, 26(7): 404–406.
64. Zhou HM, Shen Y, Wang ZJ, Li L, Zheng YF, Hakkinen L, et al. In vitro cytotoxicity evaluation of a novel root repair material. J Endod, 2013, 39(4): 478–483.
65. Zhang W, Li Z, Peng B. Effects of iRoot SP on mineralization-related genes expression in MG63 cells. J Endod, 2010, 36(12): 1978–1982.
66. Ciasca M, Aminoshariae A, Jin G, Montagnese T, Mickel A. A comparison of the cytotoxicity and proinflammatory cytokine production of EndoSequence root repair material and ProRoot mineral trioxide aggregate in human osteoblast cell culture using reverse-transcriptase polymerase chain reaction. J Endod, 2012, 38(4): 486–489.
67. Min KS, Yang SH, Kim EC. The combined effect of mineral trioxide aggregate and enamel matrix derivative on odontoblastic differentiation in human dental pulp cells. J Endod, 2009, 35(6): 847–851.
68. Woo SM, Hwang YC, Lim HS, Choi NK, Kim SH, Kim WJ, et al. Effect of nifedipine on the differentiation of human dental pulp cells cultured with mineral trioxide aggregate. J Endod, 2013, 39(6): 801–805.
69. Moghaddame-Jafari S, Mantellini MG, Botero TM, McDonald NJ, Nor JE. Effect of ProRoot MTA on pulp cell apoptosis and proliferation in vitro. J Endod, 2005, 31(5): 387–391.
70. Bonson S, Jeansonne BG, Lallier TE. Root-end filling materials alter fibroblast differentiation. J Dent Res, 2004, 83(5): 408–413.
71. Yasuda Y, Ogawa M, Arakawa T, Kadowaki T, Saito T. The effect of mineral trioxide aggregate on the mineralization ability of rat dental pulp cells: an in vitro study. J Endod, 2008, 34(9): 1057–1060.
72. Perinpanayagam H. Cellular response to mineral trioxide aggregate root-end filling materials. J Can Dent Assoc, 2009, 75(5): 369–372.
73. Torabinejad M, Hong CU, Lee SJ, Monsef M, Pitt Ford TR. Investigation of mineral trioxide aggregate for root-end filling in dogs. J Endod, 1995, 21(12): 603–608.
74. Nekoofar MH, Aseeley Z, Dummer PM. The effect of various mixing techniques on the surface microhardness of mineral trioxide aggregate. Int Endod J, 2010, 43(4): 312–320.
75. Basturk FB, Nekoofar MH, Gunday M, Dummer PM. The effect of various mixing and placement techniques on the compressive strength of mineral trioxide aggregate. J Endod, 2013, 39(1): 111–114.
76. DeAngelis L, Chockalingam R, Hamidi-Ravari A, Hay S, Lum V, Sathorn C, et al. In vitro assessment of mineral trioxide aggregate setting in the presence of interstitial fluid alone. J Endod, 2013, 39(3): 402–405.
77. Parirokh M, Torabinejad M. In: Torabinejad M, editor. Mineral trioxide aggregate: properties and clinical applications. 2014, 309–311.
78. DeLong C, He J, Woodmansey KF. The effect of obturation technique on the push-out bond strength of calcium silicate sealers. J Endod, 2015, 41(3): 385–388.
14. 2. 2018
Print: LKS. 2018; 28(2): 37 – 43
Autoři:
Rubrika:
Téma: